
【题目】在“冰→液体水→氢气和氧气”的变化过程中,微粒间被破坏的作用力依次是( )
A.范德华力、范德华力
B.范德华力、共价键
C.共价键、范德华力
D.共价键、共价键
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案科目:高中化学 来源: 题型:
【题目】在两个密闭容器甲、乙中,依次充入氧原子数目相同的O2、O3两种气体,若它们的温度和密度均相同。下列说法正确的是
A. 气体体积:甲>乙 B. 气体的压强:甲>乙
C. 气体的分子数:甲<乙 D. 气体的质量:甲<乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下说法正确的是( )
A.干冰升华克服了分子间作用力,没有破坏共价键
B.HCl气体溶于水,形成稀盐酸,仅克服分子间作用力
C.C60与金刚石互为同素异形体,它们都属于原子晶体
D.乙醇和二甲醚分子都是C2H6O,它们是同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A——F是中学化学常见的六种物质,它们之间有如下转化关系。

已知A是厨房中常见的一种调味品,D是一种黄绿色气体单质,F是一种黑色固体,F常用作催化剂,回答下列各题:
(1)①②③④四个反应中,属于氧化还原反应的是____________。
(2)写出①③两个化学反应的化学方程式:①____________________________________;③____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,体积为1mL、浓度均为0.1mol·L-1的两种常见物质X(OH)n、K2AO3的溶液分別加水稀释至体积为VmL,pH随lgV的变化情况如下图所示。下列叙述错误的是( )
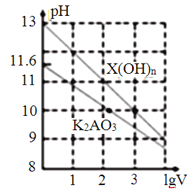
A. n=1
B. H2AO3的二级电离常数Ka2约为1.0×10-10.2
C. pH=10的两种溶液中水的电离程度相同
D. 升高温度,K2AO3溶液pH增大,X(OH)n溶液pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)3.4g NH3中含有________mol H。
(2)标准状况下,等体积的CO和CO2的质量比为________。
(3)100 mL Al2(SO4)3溶液中c (Al3+)=0.20 mol·Lˉ1,则c(SO42-)=_______。
(4)物质的量浓度相同的NaCl、MgCl2、AlCl3溶液中分别加入足量的AgNO3溶液中,生成沉淀的质量相等,三种溶液的体积比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 非金属元素形成的离子一定是阴离子
B. 非金属单质在氧化还原反应中一定是氧化剂
C. 某元素从化合态变为游离态时,一定被还原
D. 金属阳离子被还原不一定得到金属单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设 NA 代表阿伏加德罗常数的数值,下列说法正确的是
A. 2.4 g 金属镁变成镁离子时失去的电子数目为 0.1NA
B. 18 g 水中含有 0.1NA 个水分子
C. 22.4 L 氮气所含的电子数目为 NA
D. 17 g 氨气所含电子数目为 10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W原子序数依次增大。X氢化物的水溶液显碱性;Y在元素周期表中所处的周期序数与族序数相等;Z单质是将太阳能转化为电能的常用材料;W是重要的“成盐元素”,主要以钠盐的形式存在于海水中。请回答:
(l)Y在元素周期表中的位置是__________;X氢化物的电子式是__________。
(2)X氢化物的水溶液与W氢化物的水溶液混合后恰好反应时,溶液呈__________(填“酸”、“碱”或“中”)性,用离子方程式表示其原因是__________。
(3)Y-AgO电池是应用广泛的鱼雷电池,其原理如下图所示。
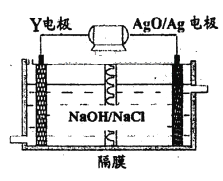
该电池的负极反应式是__________。
(4)Z和W比较,非金属性较弱的是__________(填元素符号),下列可以验证这一结论的是__________(填序号)。
a.元素在地壳中的含量
b.最高价氧化物对应水化物的酸性
c.断开氢化物中1molH-Z或H-W键所需的能量
d.Z与W以共价键形成化合物时,Z或W显示的电性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com