
 ,下列说法正确的是( )
,下列说法正确的是( )| A、苹果酸中能发生酯化反应的官能团有2种 |
| B、1 mol苹果酸可与3 mol NaOH发生中和反应 |
| C、1 mol苹果酸与足量金属Na反应生成1 mol H2 |
D、 与苹果酸互为同分异构体 与苹果酸互为同分异构体 |
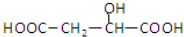 与苹果酸是同一种物质,故D错误;
与苹果酸是同一种物质,故D错误;

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
| A、16O2与18O2互为同位素,H2O、D2O、T2O互为同素异形体,N60和N2互为同系物 |
| B、除稀有气体外的非金属元素都能生成不同价态的含氧酸 |
| C、非金属元素R所形成的含氧酸盐(MaROb)中的R元素必定呈现正价 |
D、Ca的原子结构示意图为 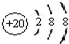 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钡原子的核外电子排布 |
| B、钡元素在周期表中的位置 |
| C、钡原子的核电荷数 |
| D、钡元素的相对原子质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解精炼铜时,同一时间内阳极溶解铜的质量与阴极析出铜的质量相等 |
| B、合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
| C、过程的自发性不仅能用于判断过程的方向,还能确定过程是否一定能发生 |
| D、S(g)+O2(g)=SO2(g)△H1,S(s)+O2(g)=SO2(g)△H2;则△H1<△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲为Fe丙为 Fe2O3 |
| B、甲为F2丙为O2 |
| C、甲为KH丙为 H2 |
| D、甲为CaC2丙为C2H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、K+、OH-、Cl- |
| B、Na+、Cu2+、SO42-、NO3- |
| C、Mg2+、Na+、SO42-、Cl- |
| D、K+、Na+、NO3-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 浓H2SO4 |
| △ |
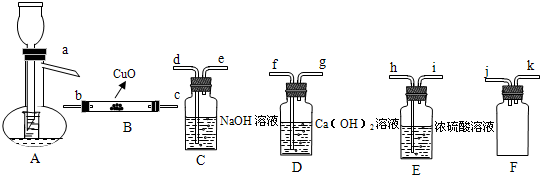
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com