
ij�о���ѧϰС�����÷Ͼ�Ǧ�����������������------Ǧ�ࣨ��PbO��PbO2��PbSO4���Ʊ����Ե�������λ�����Ǧ��3PbO•PbSO4•H2O����������Դ�����о������ʵ���������£�

��1�������Ǧ����PbSO4��Na2CO3��Һ��Ӧת��ΪPbCO3��˵���ܽ�ȣ�PbSO4 �������������PbCO3��
��2���������PbO2ת��ΪPbCO3�����ӷ���ʽ�ǣ�����ƽ�����ӷ���ʽ����






 PbO2�� SO32���� CO32���� �� PbCO3���� SO42���� OH����
PbO2�� SO32���� CO32���� �� PbCO3���� SO42���� OH����
��3��������ٺܵ͢���Һ�ϲ������� PH��7���پ��� ����ȴ�ᾧ��
��ϴ�ӡ�����ɻ��Na2SO4•10H2O���塣
��4����Ǧ�������Ϊ78g���������PbO2��PbSO4ȫ��ת��ΪPbCO3����PbOδ������Ӧ��������й��ռ���5.6LCO2(��״̬)��������л��90.9 g PbSO4,��Ǧ����PbO����������Ϊ ������������ԭ������ʧ����
 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʳƷ�������ϣ�Ҫ��Ⱦ����������������ϵ�ԭ��ͨ����
A������ B������ C������ϩ D��������ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪HCO3�D+AlO2�D +H2O=CO32�D +Al(OH)3������������KHCO3��Һ���ϵ��뺬�����ʵ�����KOH��Ba(OH)2��KAlO2�Ļ����Һ�У����ɳ��������ʵ���������KHCO3��Һ����Ĺ�ϵ�ɱ�ʾΪ


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������У�����ˮ�����Ƶ�Cu(OH)2����Һ��Na2CO3�������ƶ�����Ӧ���ǣ� ��
A���Ҵ� B����ȩ C������ D����ϩ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
˫���㶹����ҽѧ����������������ṹ��ͼ��ʾ�������йظ����ʵ�˵������ȷ���ǣ� ��
A������ʽΪC19H14O6
B����FeCl3��Һ�ܷ�����ɫ��Ӧ
C��1 mol�������������8 mol���������ӳɷ�Ӧ
D��1 mol�������������2 mol����������ȫ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ᣨHCN��������������,����֤������������ʵ���
A��HCN������ˮ
B��HCN��Һ�ܵ���
C��1mol/L��������Һ��pHԼΪ3
D��10 mL1 mol��L-1HCNǡ����10 mL 1 mol��L-1 NaOH��Һ��ȫ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������������������ԭ��Ӧ��
��2FeCl3��2KI===2FeCl2��2KCl��I2
��2FeCl2��Cl2===2FeCl3
��2KMnO4��16HCl===2KCl��2MnCl2��5Cl2����8H2O
��ij��Һ����Fe2����I����Cl�����棬Ҫ��ȥI����������Fe2����Cl������ɼ�����Լ���
A��Cl2 B��KMnO4 C��HCl D��FeCl3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ͼ��ʾΪ��Ԫ�����ڱ��е�һ���֣�����������ԭ������������XΪ35����(����)
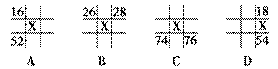
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ײʱ����ȫ�����з�����Ӧ10NaN3+2KNO3 = K2O+5Na2O+16N2��������������Ȼ�ԭ�����1.75mol���������ж���ȷ����( )
A.����40.0LN2����״����
B.��0.250molKNO3������
C.ת�Ƶ��ӵ����ʵ���Ϊ2.5mol
D.��������Nԭ�ӵ����ʵ���Ϊ3.75mol
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com