
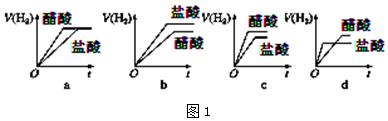
·ÖĪö £Ø1£©ŅĄ¾ŻÅäÖĘČÜŅŗĢå»żŃ”ŌńŗĻŹŹČŻĮæĘ棬ŅĄ¾Żm=CVM¼ĘĖćŠčŅŖČÜÖŹµÄÖŹĮ棻
£Ø2£©øł¾ŻÅäÖĘŅ»¶ØĪļÖŹµÄĮæÅØ¶ČµÄČÜŅŗ²½ÖčŃ”ÓĆŅĒĘ÷£¬Č»ŗóÅŠ¶Ļ»¹Č±ÉŁµÄŅĒĘ÷£»
£Ø3£©ŅĄ¾ŻC=$\frac{1000¦Ń¦Ų}{M}$¼ĘĖćÅØĮņĖįµÄĪļÖŹµÄĮæÅØ¶Č£¬ŅĄ¾ŻČÜŅŗĻ”ŹĶ¹ż³ĢÖŠČÜÖŹµÄĪļÖŹµÄĮæ²»±ä¼ĘĖćŠčŅŖÓĆĮņĖįĢå»ż£¬ŅĄ¾ŻÅØĮņĖįĢå»żŃ”ŌńŗĻŹŹ¹ęøńµÄĮæĶ²£»
£Ø4£©·ÖĪö²Ł×÷¶ŌČÜÖŹµÄĪļÖŹµÄĮæŗĶČÜŅŗĢå»żµÄÓ°Ļģ£¬ŅĄ¾ŻC=$\frac{n}{V}$½ųŠŠĪó²ī·ÖĪö£®
½ā“š ½ā£ŗ£Ø1£©¹ĢĢåÉÕ¼īÅäÖĘ0.4mol/LµÄNaOHČÜŅŗ480mL£¬Ó¦Ń”Ōń500mLČŻĮæĘ棬Źµ¼ŹÅäÖĘ500mLČÜŅŗ£¬ŠčŅŖĒāŃõ»ÆÄĘÖŹĮæ£ŗ0.4mol/L”Į0.5L”Į40g/mol=8.0g£»
¹Ź“š°øĪŖ£ŗ8.0£»
£Ø2£©Ć»ÓŠ¹ęøńĪŖ480mLµÄČŻĮæĘ棬ÅäÖĘŹ±ŠčŅŖŃ”ÓĆ500mLµÄČŻĮæĘ棬ÅäÖĘ²½ÖčĪŖ£ŗ¼ĘĖć”¢³ĘĮæ£ØĮæČ”£©”¢Čܽā£ØĻ”ŹĶ£©”¢ĄäČ“”¢×ŖŅĘ”¢Ļ“µÓ”¢¶ØČŻ”¢Ņ”ŌČµČ£¬ŠčŅŖŹ¹ÓƵÄŅĒĘ÷ÓŠ£ŗĶŠÅĢĢģĘ½£ØĮæĶ²£©”¢²£Į§°ō”¢ÉÕ±”¢Ņ©³×”¢500mLČŻĮæĘ攢½ŗĶ·µĪ¹ÜµČ£¬ĖłŅŌ±ŲŠėÓƵ½µÄŅĒĘ÷£ŗ¢Ł¢Ś¢Ü¢Ż¢Ž¢ß£»»¹Č±ÉŁµÄŅĒĘ÷£ŗ»¹Č±ÉŁµÄ²£Į§ŅĒĘ÷ĪŖ£ŗ½ŗĶ·µĪ¹Ü£»
¹Ź“š°øĪŖ£ŗ¢Ł¢Ś¢Ü¢Ż¢Ž¢ß£»½ŗĶ·µĪ¹Ü£»
£Ø3£©98%”¢ĆܶČĪŖ1.84g/cm3µÄÅØĮņĖįĪļÖŹµÄĮæÅضČC=$\frac{1000”Į1.84”Į98%}{98}$=18.4mol/L£¬ÉčŠčŅŖÅØĮņĖįĢå»żĪŖV£¬ŌņŅĄ¾ŻČÜŅŗĻ”ŹĶ¹ż³ĢÖŠČÜÖŹµÄĪļÖŹµÄĮæ²»±äµĆ£ŗ18.4mol/L”ĮV=0.5mol/L”Į500mL£¬½āµĆV=13.6mL£¬ĮæČ”13.6mLČÜŅŗ£¬Ó¦Ń”Ōń15mLĮæĶ²£»
¹Ź“š°øĪŖ£ŗ13.6£»15£»
£Ø4£©¢ŁĪ“Ļ“µÓÉÕ±”¢²£Į§°ō£¬µ¼ÖĀČÜÖŹµÄĪļÖŹµÄĮæĘ«Š”£¬ČÜŅŗÅضČĘ«µĶ£¬¹Ź²»Ń”£»
¢Ś³ĘĮæNaOHµÄŹ±¼äĢ«³¤£¬µ¼ÖĀ³ÓČ”µÄ¹ĢĢåÖŠĒāŃõ»ÆÄĘÖŹĮæĘ«Š”£¬ČÜÖŹµÄĪļÖŹµÄĮæĘ«Š”£¬ČÜŅŗÅضČĘ«µĶ£¬¹Ź²»Ń”£»
¢Ū¶ØČŻŹ±ø©ŹÓæĢ¶Č£¬µ¼ÖĀČÜŅŗĢå»żĘ«Š”£¬ČÜŅŗÅضČĘ«øߣ¬¹ŹŃ”£»
¢ÜČŻĮæĘæ²»øÉŌļ£¬ŗ¬ÓŠÉŁĮæÕōĮóĖ®£¬¶ŌČÜÖŹµÄĪļÖŹµÄĮæŗĶČÜŅŗĢå»ż¶¼²»²śÉśÓ°Ļģ£¬ČÜŅŗÅØ¶Č²»±ä£¬¹Ź²»Ń”£»
¢ŻNaOHČÜŅŗĪ“ĄäČ“ÖĮŹŅĪĀ¾Ķ×ŖŅʵ½ČŻĮæĘ棬ĄäČ“ŗó£¬ČÜŅŗĢå»żĘ«Š”£¬ČÜŅŗÅضČĘ«øߣ¬¹ŹŃ”£»
¢ŽĮæČ”ÅØĮņĖįŹ±£¬ŃöŹÓĮæĶ²æĢ¶ČĻߣ¬µ¼ÖĀĮæČ”ÅØĮņĖįĢå»żĘ«“ó£¬ČÜÖŹµÄĪļÖŹµÄĮæĘ«“ó£¬ČÜŅŗÅضČĘ«øߣ¬¹ŹŃ”£»
¹ŹŃ”£ŗ¢Ū¢Ż¢Ž£®
µćĘĄ ±¾Ģāæ¼²éĮĖÅäÖĘŅ»¶ØĪļÖŹµÄĮæÅØ¶ČµÄČÜŅŗµÄ·½·Ø£¬ĢāÄæÄŃ¶Č²»“ó£¬Ć÷Č·ÅäÖĘ²½ÖčĪŖ½ā“š¹Ų¼ü£¬×¢ŅāÕĘĪÕÅäÖĘ¹ż³ĢÖŠĪó²ī·ÖĪöµÄ·½·ØÓė¼¼ĒÉ£¬ŹŌĢāÓŠĄūÓŚÅąŃųѧɜµÄ»ÆѧŹµŃéÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.42mol•L-1 | B£® | 0.21mol•L-1 | C£® | 0.56mol•L-1 | D£® | 0.24mol•L-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½« 100mL 0.1 mol•L-1µÄFeCl3ČÜŅŗµĪČė·ŠĖ®ÖŠæÉÖʵĆFe£ØOH£©3½ŗĮ£ŹżÄæĪŖ0.01NA | |
| B£® | Ķس£×“æöĻĀ£¬0.5 molŠæĮ£Óė×ćĮæŃĪĖį·“Ó¦²śÉś11.2 L H2 | |
| C£® | ³£ĪĀ³£Ń¹ĻĀ£¬2.4g½šŹōĆ¾±ä³ÉĆ¾Ąė×ÓŹ±£¬Ź§Č„µÄµē×ÓŹżĪŖ0.1NA | |
| D£® | ±ź×¼×“æöĻĀ£¬22.4LÓÉN2ŗĶN2O×é³ÉµÄ»ģŗĻĘųĢåÖŠ£¬Ėłŗ¬NŌ×ÓµÄøöŹżĪŖ2NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| K1 | K2 | |
| H2SO3 | 1.54”Į10-2 | 1.02”Į10-7 |
| H2CO3 | 4.3”Į10-7 | 5.6”Į10-11 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
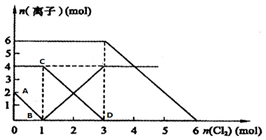 ĻņFeI2”¢FeBr2µÄ»ģŗĻČÜŅŗÖŠĶØČėŹŹĮæĀČĘų£¬ČÜŅŗ֊ijŠ©Ąė×ÓµÄĪļÖŹµÄĮæ±ä»ÆČēĶ¼ĖłŹ¾£®
ĻņFeI2”¢FeBr2µÄ»ģŗĻČÜŅŗÖŠĶØČėŹŹĮæĀČĘų£¬ČÜŅŗ֊ijŠ©Ąė×ÓµÄĪļÖŹµÄĮæ±ä»ÆČēĶ¼ĖłŹ¾£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H2SO4ØT2H++S6++4O2- | B£® | HNO3ØTH++NO3- | ||
| C£® | Ba£ØOH£©2ØTBa2++OH- | D£® | Na2CO3ØTNa2++CO32- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com