

 。
。 )B的稀溶液与AgNO3溶液混合可形成沉淀AgX,此沉淀的Ksp(AgX) =1.8×10-10。将等体积的B稀溶液与AgNO3溶液混合,若B的浓度为2×10—4
)B的稀溶液与AgNO3溶液混合可形成沉淀AgX,此沉淀的Ksp(AgX) =1.8×10-10。将等体积的B稀溶液与AgNO3溶液混合,若B的浓度为2×10—4 mo1/L
mo1/L  ,则生成沉淀所需AgNO3溶液的最小浓度为________。若向AgX悬浊液中滴加KI溶液,观察到的现象 ,沉淀能够发生转化的原因是 。
,则生成沉淀所需AgNO3溶液的最小浓度为________。若向AgX悬浊液中滴加KI溶液,观察到的现象 ,沉淀能够发生转化的原因是 。科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 C D
C D 查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
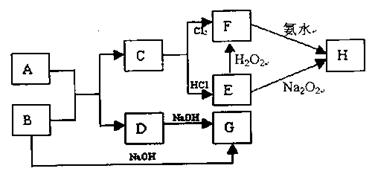
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 —、Cl—、NO3—中的一种或几种,取该溶液进行连续实验,实验过程如下:
—、Cl—、NO3—中的一种或几种,取该溶液进行连续实验,实验过程如下: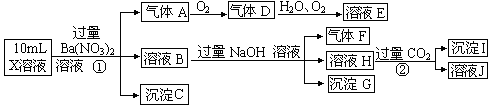
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铯与冷水反应十分平缓并生成H2 |
| B.铯与硫酸反应,生成CsSO4与H2 |
| C.铯的氧化物可直接与水反应生成CsOH |
| D.铯在空气中燃烧生成Cs2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com