
A.5∶3 B.5∶4 C.1∶1 D.3∶5
科目:高中化学 来源: 题型:阅读理解
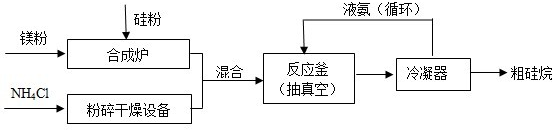
 (2013?海淀区二模)氮化硅膜与二氧化硅膜相比较具有表面化学性能稳定等优点,故氮化硅膜可用于半导体工业.为生成氮化硅膜,可以用NH3和SiH4(硅烷)在一定条件下反应并在600℃的加热基板上生成氮化硅膜:
(2013?海淀区二模)氮化硅膜与二氧化硅膜相比较具有表面化学性能稳定等优点,故氮化硅膜可用于半导体工业.为生成氮化硅膜,可以用NH3和SiH4(硅烷)在一定条件下反应并在600℃的加热基板上生成氮化硅膜:
| ||
| ||


| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源:上海市宝山区2013年高考一模化学试题 题型:022
硝酸盐受热分解的产物与硝酸盐的组成以及受热的温度等因素有关.
Ⅰ.一定条件下硝酸铵受热分解的化学反应方程式为:NH4NO3→HNO3+N2 +H2O(未配平)
1.该反应中发生还原反应的过程是________→________.
2.反应中被氧化与被还原的氮原子数之比为________;现有1 mol NH4NO3分解,生成的氧化产物的物质的量是________mol.
Ⅱ.硝酸铵受撞击或高温发生爆炸的化学反应方程式为:mNH4NO3→nO2+pN2+qH2O
3.下列关于该方程式中化学计量数的说法正确的是________(选填字母编号).
a.m=1
b.n=2
c.p=3
d.q=4
4.若反应过程中共转移3.01×1023个电子,则反应可产生气体的体积为________(标准状况).
查看答案和解析>>
科目:高中化学 来源:2012-2013学年上海市宝山区高三上学期期末教学质量调研化学试卷(解析版) 题型:填空题
硝酸盐受热分解的产物与硝酸盐的组成以及受热的温度等因素有关。
Ⅰ.一定条件下硝酸铵受热分解的化学反应方程式为:NH4NO3→HNO3+N2 +H2O(未配平)
(1)该反应中发生还原反应的过程是_______→________。
(2)反应中被氧化与被还原的氮原子数之比为__________;现有1mol NH4NO3分解,生成的氧化产物的物质的量是 mol。
Ⅱ.硝酸铵受撞击或高温发生爆炸的化学反应方程式为:m NH4NO3→n O2+p N2+q H2O
(3)下列关于该方程式中化学计量数的说法正确的是_________(选填字母编号)。
a.m=1 b.n=2 c.p=3 d.q=4
(4)若反应过程中共转移3.01×1023个电子,则反应可产生气体的体积为_____(标准状况)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com