
����Ŀ��ijһ��Ӧ��ϵ�з�Ӧ��������ﹲ�������ʣ�O2��H2CrO4��Cr(OH)3��H2O��H2O2����֪�÷�Ӧ��H2O2ֻ�������¹��̣�H2O2��O2��
��1���÷�Ӧ�еĻ�ԭ����____________��
��2���÷�Ӧ�У�������ԭ��Ӧ�Ĺ�����____________��____________��
��3��д���÷�Ӧ�Ļ�ѧ����ʽ�����������ת�Ƶķ������Ŀ____________��
��4���練Ӧת����0.3 mol���ӣ�������������ڱ�״�������Ϊ_______��
���𰸡�H2O2 H2CrO4 Cr(OH)3 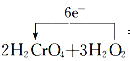 =2Cr��OH��3��+3O2��+2H2O 3.36L
=2Cr��OH��3��+3O2��+2H2O 3.36L
��������
��H2O2��O2��֪����Ӧ��OԪ�صĻ��ϼ����߱�������CrԪ�صĻ��ϼ۽��ͱ���ԭ����Ӧ��H2O2�ǻ�ԭ����H2CrO4Ϊ��������
��1����H2O2��O2��֪����Ӧ��OԪ�صĻ��ϼ����߱���������Ӧ��H2O2�ǻ�ԭ�����ʴ�Ϊ��H2O2��
��2����H2O2��O2��֪����Ӧ��OԪ�صĻ��ϼ����ߣ���CrԪ�صĻ��ϼ۽��ͱ���ԭ�� H2CrO4Ϊ��������Cr��OH��3Ϊ��ԭ�����ԭ��Ӧ�Ĺ���ΪH2CrO4��Cr��OH��3���ʴ�Ϊ��H2CrO4��Cr��OH��3��
��3���÷�Ӧ��OԪ��ʧ���ӣ�CrԪ�صõ����ӣ�2molH2CrO4��Ӧת�Ƶ���Ϊ2mol����6-3��=6mol�����õ����ŷ��������ת�Ƶķ������ĿΪ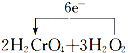 =2Cr��OH��3��+3O2��+2H2O���ʴ�Ϊ��
=2Cr��OH��3��+3O2��+2H2O���ʴ�Ϊ��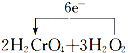 =2Cr��OH��3��+3O2��+2H2O��
=2Cr��OH��3��+3O2��+2H2O��
��4���ɷ�Ӧ2H2CrO4+3H2O2�T2Cr��OH��3��+3O2��+2H2O��֪������3mol����ת��6mol���ӣ���ת����0.3mol���ӣ����������������ʵ���Ϊ0.3mol��6��3=0.15mol�����ڱ�״�������Ϊ0.15mol��22.4L/mol=3.36L���ʴ�Ϊ��3.36L��


 ����ѧ����ϵ�д�
����ѧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�ǹ�ҵ��ⱥ��ʳ��ˮ��װ��ʾ��ͼ�������й�˵���в���ȷ����
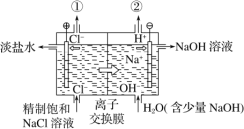
A.װ���з�����Ӧ�����ӷ���ʽΪ2Cl-+2H+![]() H2��+Cl2��
H2��+Cl2��
B.װ���г�����������������������������������������
C.�����ӽ���Ĥֻ����������ͨ����������������ͨ��
D.��װ���ǽ�����ת��Ϊ��ѧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���Һ�У�Na+���ʵ���Ũ�������ǣ�������
A. 4 L��0.5 mol��L-1NaCl��Һ B. 1 L��0.3 mol��L-1Na2SO4��Һ
C. 5 L��0.4 mol��L-1NaOH��Һ D. 2 L��0.15 mol��L-1��Na3PO4��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ�������µĻ�ѧƽ��H2(g)+I2(g)![]() 2HI(g) ��H��0������˵����ȷ���ǣ� ��
2HI(g) ��H��0������˵����ȷ���ǣ� ��
A.���º��ݣ�����H2��v����������ƽ������
B.���º��ݣ�����He��v����������ƽ������
C.��ѹ��v��������v���棩���䣬ƽ�ⲻ�ƶ�
D.���£�v��������С��v���棩����ƽ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪһ��������ͼ����С����ͼ���Ϸֱ�д��H2��CO2��Na2O��NaCl��FeCl3�������ʣ�ͼ���������������ʾ��ɹ���Ϊһ�࣬�ཻ����A��B��C��DΪ����Ӧ�ķ������ݴ��š���ش��������⣺

(1)�뽫�������ݴ���������Ӧ�������ڣ�
��__________���������ʶ����ǵ����
��__________���������ʶ����ƵĻ�����
��__________���������ʶ���������
��__________���������ʶ�����
(2)�ýྻ���ձ�ȡ��������ˮ���þƾ��Ƽ��������ڣ����ձ�����μ���1 mol/L����ͼ��ij������M��ˮ��Һ��������п��Ƶ�һ�ֺ��ɫ���塣
������M�Ļ�ѧʽΪ______________��
��֤���к��ɫ�������ɵ�ʵ��ԭ����_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£������Ϊ3 L���ܱ������У�һ����̼��������Ӧ���ɼ״�(����ΪCu2O/ZnO)��CO(g)��2H2(g)CH3OH(g)��
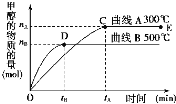
��������������и��⣺
(1)��Ӧ�ﵽƽ��ʱ��ƽ�ⳣ������ʽK��__________�������¶ȣ�Kֵ__________(����������������С������������)��
(2)��500�棬�ӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v(H2)��______________��
(3)�������������������£��Դ���E�����ϵ���ѹ����ԭ����1/2�������йظ���ϵ��˵����ȷ����__________(����ĸ���)��
a.������Ũ�ȼ�С b.����Ӧ���ʼӿ죬�淴Ӧ����Ҳ�ӿ�
c.�״������ʵ������� d.����ƽ��ʱn(H2)/n(CH3OH)����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ܶ࣬��������Ҳ�ܶࡣ![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() �����ֳ����ĺ����ijͬѧ������˼·����̽����
�����ֳ����ĺ����ijͬѧ������˼·����̽����
(1)���ࣺ�����ᡢ��Ρ���������з��࣬�����������������εĹ���______�֣�������Ԫ�ػ��ϼ���ͬ�����ʷ�Ϊһ�࣬�����������ʿɷ�Ϊ______�ࡣ
(2)������к�������ת����д����Ӧ�Ļ�ѧ����ʽ���Լ�����ѡ����
![]() ��______��
��______��
![]() ��______��
��______��
![]() ��______��
��______��
(3)Ϊ����![]() ����Ⱦ�����Ϊ�����ҹ�����̽����һ����������
����Ⱦ�����Ϊ�����ҹ�����̽����һ����������![]() ��ԭ
��ԭ![]() �õ�������ķ�������ȥ
�õ�������ķ�������ȥ![]() ���÷�Ӧ�Ļ�ѧ����ʽΪ____________��
���÷�Ӧ�Ļ�ѧ����ʽΪ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�����Ⱥ����ܱ�������ͨ��CO(g)��H2O(g)��һ��������ʹ��ӦCO(g)��H2O(g)![]() CO2(g)��H2(g)�ﵽƽ�⣬����Ӧ������ʱ��仯��������ͼ��ʾ����ͼ�ɵó��Ľ�����ȷ����
CO2(g)��H2(g)�ﵽƽ�⣬����Ӧ������ʱ��仯��������ͼ��ʾ����ͼ�ɵó��Ľ�����ȷ����

A. ��Ӧ��Ũ�ȣ�a��С��c��
B. �÷�Ӧ������ӦΪ���ȷ�Ӧ
C. c��ﵽƽ��״̬
D. ��t1����t2ʱ��H2�IJ��ʣ�a��b�δ���b��c��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1 L FeCl3��CuCl2�Ļ����Һ������Cu2+Ũ��Ϊ0.05 mol��L��1���м���һ������Fe�ۣ���ַ�Ӧ����ˣ�ʣ���������Ϊ6.0 g������Һ�м���������AgNO3��Һ������57.4 g����������˵����ȷ����
A.ʣ�����ΪCuB.����Fe�۵�����Ϊ8.4 g
C.ԭ��Һ��Fe3+Ũ��Ϊ0.3 mol��L��1D.��Ӧ����Һ��Fe2+Ũ��Ϊ0.2 mol��L��1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com