
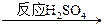 CuSO4。②由Cu
CuSO4。②由Cu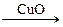 CuSO4,试回答:
CuSO4,试回答: CuSO4+SO2↑+2H2O 2Cu+O2
CuSO4+SO2↑+2H2O 2Cu+O2 2CuO
2CuO CuSO4+SO2↑+2H2O,方案②先将铜变为CuO,方程式为2Cu+O2
CuSO4+SO2↑+2H2O,方案②先将铜变为CuO,方程式为2Cu+O2 2CuO,CuO再与硫酸作用生成CuSO4,方程式为CuO+H2SO4====CuSO4+H2O。(2)方案②较合理,因为由方程式可知,生成等质量的硫酸铜,所用Cu的质量相同,而耗硫酸的质量方案①是方案②的2倍,方案②节约原料;从环境保护角度看,方案①有SO2有毒气体生成,污染环境,而方案②不会造成环境污染。
2CuO,CuO再与硫酸作用生成CuSO4,方程式为CuO+H2SO4====CuSO4+H2O。(2)方案②较合理,因为由方程式可知,生成等质量的硫酸铜,所用Cu的质量相同,而耗硫酸的质量方案①是方案②的2倍,方案②节约原料;从环境保护角度看,方案①有SO2有毒气体生成,污染环境,而方案②不会造成环境污染。

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源:不详 题型:实验题
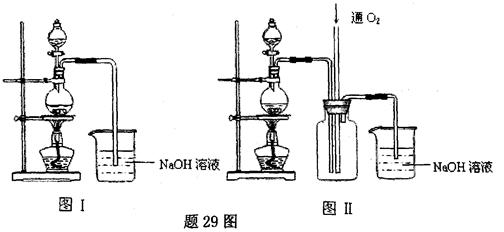
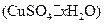 晶体中结晶水的含量时.测得有关数据如下表:
晶体中结晶水的含量时.测得有关数据如下表:| 加热前质量 | 加热后质量 | |
| m1(容器) | m2(容器+晶体) | m3(容器+无水CuSO4) |
| 5.4g | 7.9g | 6.8g |
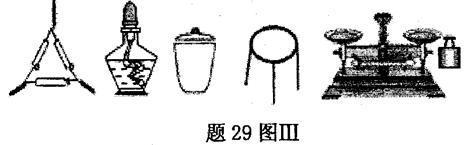
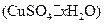 中结晶水含量的实验中,称量操作至少进行 次。
中结晶水含量的实验中,称量操作至少进行 次。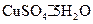 相比
相比 ) (填“偏高”、“偏低”、“不变”),可能的原因是 。(填字母序号)
) (填“偏高”、“偏低”、“不变”),可能的原因是 。(填字母序号)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①④⑥ |
| B.③⑤⑦ |
| C.②④⑤ |
| D.②⑥⑦ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
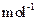 :MnCO3 115 MnO2 87 MnO 71)
:MnCO3 115 MnO2 87 MnO 71)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
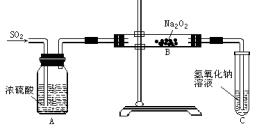

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.a∶b | B.a∶2b | C.a∶(a+2b) | D.a∶2(a+b) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com