
 某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2.
某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2.分析 本题利用实验室制备的氯气及二氧化硫制取SO2Cl2,因SO2Cl2常温下为无色液体,极易水解,遇潮湿空气会产生白雾,因此氯气和二氧化硫都需要经过除杂及干燥处理,氯气通常使用浓硫酸干燥,探究反应产物的性质,涉及到反应原理水解产物的检验,主要是检验SO42-和Cl-,其中Cl-的检验一定要利用硝酸钡除去溶液里的SO42-,排除干扰,据此分析解题;
I.根据在化合物中,元素化合价的代数和为零进行解答;
Ⅱ.浓硫酸具有吸水性,可以干燥氯气;
Ⅲ.(1)①SO2Cl2与H2O反应生成硫酸和氯化氢;
②氯离子与银离子反应生成不溶液硝酸的氯化银沉淀,注意应先加入硝酸钡溶液,先排除硫酸根离子的干扰;
(2)SO2和Cl2生成SO2Cl2的反应为可逆反应,SO2Cl2分解得到的氯气和二氧化硫在水溶液中发生氧化还原反应生成硫酸和氯化氢,硫酸与氯化钡反应生成硫酸钡沉淀,SO2和Cl2生成SO2Cl2的反应为可逆反应.
解答 解:I.SO2Cl2中,氧为-2价,氯为-1价,根据在化合物中,元素化合价的代数和为零可知硫元素化合价为+6价;
故答案为:+6价;
II.要收集干燥的氯气应除去氯气中的水蒸气,选用浓硫酸可以干燥氯气;
故答案为:浓硫酸;
Ⅲ.(1)SO2Cl2与水反应的方程式:①SO2Cl2+2H2O=H2SO4+2HCl;
故答案为:SO2Cl2+2H2O=H2SO4+2HCl;
②要检验溶液中的氯离子应排除硫酸根离子的干扰,所以:取少量该溶液于试管中,加入过量Ba(NO3)2溶液,过滤,向滤液中滴加HNO3酸化,再加入AgNO3溶液,若产生白色沉淀,则说明溶液中有Cl-;
故答案为:取少量该溶液于试管中,加入过量Ba(NO3)2溶液,过滤,向滤液中滴加HNO3酸化,再加入AgNO3溶液,若产生白色沉淀,则说明溶液中有Cl-;
(2)SO2和Cl2生成SO2Cl2的反应为可逆反应,SO2Cl2分解得到的氯气和二氧化硫在水溶液中发生氧化还原反应生成硫酸和氯化氢,硫酸与氯化钡反应生成硫酸钡沉淀,SO2和Cl2生成SO2Cl2的反应为可逆反应,化学方程式为:SO2+Cl2=SO2 Cl2;
故答案为:①BaSO4;②SO2+Cl2=SO2 Cl2.
点评 本题为实验题,考查了二氧化硫的性质,题目难度中等,明确物质的性质是解题关键,注意离子检验的方法.


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:填空题
 向电解质溶液中加入新物质时,其导电性符合如图所示变化趋势的实验操作是②.
向电解质溶液中加入新物质时,其导电性符合如图所示变化趋势的实验操作是②.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 、
、 、
、 烯烃的名称:
烯烃的名称:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Br2 | B. | I2和 KCl | C. | I2.KCl和NaCl | D. | KCl和NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑤ | B. | ②③④ | C. | ①③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
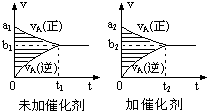 可逆反应mA(g)+nB(g)?pC(g)+qD(g)的v-t图象如图,若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如图.对于下列命题:
可逆反应mA(g)+nB(g)?pC(g)+qD(g)的v-t图象如图,若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如图.对于下列命题:| A. | ②④⑤⑦ | B. | ①④⑥⑧ | C. | ②③⑤⑧ | D. | ①③⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol苯分子中含有0.3NA个碳碳双键 | |
| B. | 1L 1mol/L碳酸钠溶液中阴离子的数目大于NA | |
| C. | 标准状况下,22.4L己烷中含有的分子数共为NA | |
| D. | 50mL 18.4mol/L浓硫酸与足量铜微热反应,转移的电子数目为0.92 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com