
【题目】以下不是以石油、煤和天然气为主要原料生产的材料是
A.陶瓷B.塑料C.合成纤维D.合成橡胶
 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
【题目】铜锌合金的颜色酷似金的颜色,所以近来用铜锌合金制成的假金元宝欺骗行人的事件屡有发生。下列不易区别其真伪的方法是( )
A. 测定密度 B. 放入硝酸中 C. 放入盐酸中 D. 观察外观
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅及其化合物在材料领域中的应用广泛.下列叙述不正确的是( )
A. 硅单质可用来制造太阳能电池
B. 二氧化硅是制造光导纤维的材料
C. 石英(SiO2)可用来制作工艺品
D. 硅单质是制造玻璃的主要原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
①化石燃料在任何条件下都能充分燃烧
②化石燃料在燃烧过程中能产生污染环境的CO、SO2 等有害气体
③直接燃烧煤不如将煤进行深加工后再燃烧效果好
④固体煤变为气体燃料后,燃烧效率将更低
A.①④B.②③④C.②③D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
①Sn (s、白)+2HCl (aq)=SnCl2 (aq)+H2 (g);DH1
②Sn (s、灰)+2HCl (aq)=SnCl2 (aq)+H2 (g);DH2
③Sn (s、灰)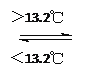 Sn (s、白);DH3=+2.1 kJ/mol
Sn (s、白);DH3=+2.1 kJ/mol
下列说法正确的是( )
A. DH1>DH2
B. 锡在常温下以灰锡状态存在
C. 灰锡转化为白锡的反应是放热反应
D. 锡制器皿长期处于低于13.2 ℃的环境中,会自行毁坏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、钴、镍等金属单质及化合物有广泛的应用。
(1)已知锂离子电池总反应方程式是FePO4(s)+Li(s) ![]() LiFePO4(s)。请写出Fe3+的电子排布式____________,PO43-离子中p原子杂化轨道类型____________。
LiFePO4(s)。请写出Fe3+的电子排布式____________,PO43-离子中p原子杂化轨道类型____________。
(2)化合物“钴酞菁”能显著提升二次电池的充放电效率,下图是改性“氨基钴酞菁”分子的结构图。
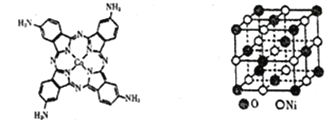
①一个电子的运动状态取决于______种因素,基态Co原子中空间运动状态不同的电子数为___种。
②氨基钴酞菁中非金属元素的电负性从大到小的顺序为_________
③“氨基钴酞菁”比“钴酞菁”显著溶于水,请简述其原因_______。
(3)K3[Co(NO2)6]中存在的化学键类型有____________,配位数为_______。
(4)Sr和Ca为同族金属元素,CaO与SrO熔点更高、硬度更大,请简述原因______。
(5)如上图所示为NiO晶体的晶胞示意图:
①该晶胞中与一个Ni最近等距离的O构成的空间几何形状为____________________。
②在NiO晶体中Ni2+的半径为apm,O3-的半径为bpm,假设它们在晶体中是紧密接触的,则其密度为___g/cm3。(用含字母a、b的计算式表达)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种气体,取X和Y按物质的量之比1∶1混合,放入某密闭容器中发生反应X+2Y![]() 2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于
2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于
A. 33% B. 40% C. 50% D. 65%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH<0
2SO3(g) ΔH<0
(1)写出该反应的化学平衡常数表达式K=_____________________。降低温度,该反应K值____________,二氧化硫转化率____________,化学反应速率___________。(以上均填“增大”“减小”或“不变”)
(2)600 ℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图所示,反应处于平衡状态的时间是_______________________________________________。
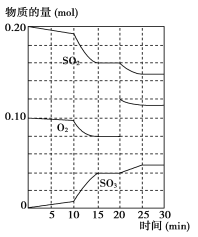
(3据上图判断,反应进行至20 min时,曲线发生变化的原因是_______________________(用文字表达);10 min到15 min的曲线变化的原因可能是__________(填写编号)。
a.加了催化剂 b.缩小容器体积
c.降低温度 d.增加SO3的物质的量
(4)已知在600℃时,2SO2(g)+O2(g) ![]() 2SO3(g)的平衡常数K=19,若600℃时测得容器内c(SO2)=0.3mol/L,c(O2)=0.1mol/L,c(SO3)=0.4mol/L,在这种情况下,该反应是否处于平衡状态?_________(填“是”或“否”)。此时,化学反应速率是v(正)_______v(逆)(填“>”、“<”或“=”),原因是________________________________________________________________________________。
2SO3(g)的平衡常数K=19,若600℃时测得容器内c(SO2)=0.3mol/L,c(O2)=0.1mol/L,c(SO3)=0.4mol/L,在这种情况下,该反应是否处于平衡状态?_________(填“是”或“否”)。此时,化学反应速率是v(正)_______v(逆)(填“>”、“<”或“=”),原因是________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在防治禽流感疫睛中大量使用的氯胺是一种长效缓释有机氯消毒剂,具有强氧化性,其杀菌能力是一般含氯消毒剂的4~5倍。下列有关氯胺(NH2Cl)的说法中一定不正确的是(______)
A氯胺的电子式为:![]()
B氯胺晶体属于分子晶体,氯化铵晶体属于离子晶体
C 氯胺水解产物为NH2OH(羟氨)和HCl
D氯胺的消毒原理与漂白粉相似
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com