
| A£® | Ba2+”¢Cu2+”¢NO3-”¢SO42- | B£® | K+”¢Na+”¢SO42-”¢Cl- | ||
| C£® | CO32-”¢H+”¢Na+”¢K+ | D£® | H+”¢Cl-”¢NO3-”¢Ag+ |
·ÖĪö øł¾ŻĄė×ÓÖ®¼ä²»ÄܽįŗĻÉś³É³Įµķ”¢ĘųĢ唢Ė®µČ£¬ŌņĄė×ÓŌŚČÜŅŗÖŠÄÜ“óĮæ¹²“ę£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗA£®Ba2+”¢CO32-·“Ӧɜ³É³Įµķ¶ų²»ÄÜ“óĮæ¹²“ę£¬¹ŹA“ķĪó£»
B£®øĆ×éĄė×ÓÖ®¼ä²»·“Ó¦£¬Äܹ»“óĮæ¹²“ę£¬¹ŹBÕżČ·£»
C£®CO32-”¢H+·“Ӧɜ³É¶žŃõ»ÆĢ¼ŗĶĖ®£¬²»ÄÜ“óĮæ¹²“ę£¬¹ŹC“ķĪó£»
D£®Cl-”¢Ag+·“Ӧɜ³É³Įµķ¶ų²»ÄÜ“óĮæ¹²“ę£¬¹ŹD“ķĪó£®
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éĄė×ӵĹ²“ęĪŹĢā£¬ĪŖøßæ¼³£¼ūĢāŠĶ£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦µÄ漲飬עŅā°ŃĪÕ³£¼ūĄė×ӵĊŌÖŹŅŌ¼°·“Ó¦ĄąŠĶµÄÅŠ¶Ļ£¬ŹģĻ¤ø“·Ö½ā·“Ó¦·¢ÉśµÄĢõ¼ž¼°³£¼ūĪļÖŹµÄČܽāŠŌ¼“æɽā“š£¬ÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µŚČżÖÜĘŚµŚ0×å | B£® | µŚĖÄÖÜĘŚµŚ¢ńA×å | C£® | µŚČżÖÜĘŚµŚ¢ńA×å | D£® | µŚČżÖÜĘŚµŚ¢÷A×å |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
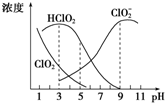 ŃĒĀČĖįÄĘŹĒŅ»ÖÖøߊ§Ńõ»Æ¼Į”¢ĘÆ°×¼Į£¬Ö÷ŅŖÓĆÓŚĆŽ·Ä”¢Ö½½¬µČĘÆ°×£¬ŃĒĀČĖįÄĘ£ØNaClO2£©ŌŚČÜŅŗÖŠæÉÉś³ÉClO2”¢HClO2”¢ClO${\;}_{2}^{-}$”¢Cl-µČ£¬ĘäÖŠHClO2ŗĶClO2¶¼¾ßÓŠĘÆ°××÷ÓĆ£¬µ«ClO2ŹĒÓŠ¶¾ĘųĢ壮¾²ā¶Ø£¬25”ꏱø÷×é·Öŗ¬ĮæĖępH±ä»ÆĒéæöČēĶ¼ĖłŹ¾£ØCl-ƻӊ»³ö£©£®ŌņĻĀĮŠ·ÖĪö“ķĪóµÄŹĒ£Ø””””£©
ŃĒĀČĖįÄĘŹĒŅ»ÖÖøߊ§Ńõ»Æ¼Į”¢ĘÆ°×¼Į£¬Ö÷ŅŖÓĆÓŚĆŽ·Ä”¢Ö½½¬µČĘÆ°×£¬ŃĒĀČĖįÄĘ£ØNaClO2£©ŌŚČÜŅŗÖŠæÉÉś³ÉClO2”¢HClO2”¢ClO${\;}_{2}^{-}$”¢Cl-µČ£¬ĘäÖŠHClO2ŗĶClO2¶¼¾ßÓŠĘÆ°××÷ÓĆ£¬µ«ClO2ŹĒÓŠ¶¾ĘųĢ壮¾²ā¶Ø£¬25”ꏱø÷×é·Öŗ¬ĮæĖępH±ä»ÆĒéæöČēĶ¼ĖłŹ¾£ØCl-ƻӊ»³ö£©£®ŌņĻĀĮŠ·ÖĪö“ķĪóµÄŹĒ£Ø””””£©| A£® | ŃĒĀČĖįÄĘŌŚ¼īŠŌĢõ¼žĻĀ½ĻĪČ¶Ø | |
| B£® | 25”ꏱ£¬HClO2µÄµēĄėĘ½ŗā³£ŹżµÄŹżŌ¼ĪŖKa=10-6 | |
| C£® | 25”ꏱ£¬Ķ¬ÅØ¶ČµÄHClO2ČÜŅŗŗĶNaClO2ČÜŅŗµČĢå»ż»ģŗĻ£ØŗöĀŌCl-£©£¬Ōņ»ģŗĻČÜŅŗÖŠÓŠc£ØHClO2£©+2c£ØH+£©ØTc£ØClO${\;}_{2}^{-}$£©+2c£ØOH-£© | |
| D£® | Ź¹ÓĆøĆĘÆ°×¼ĮµÄ×ī¼ŃpHĪŖ3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
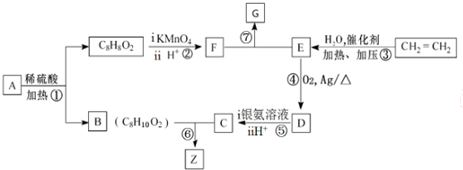
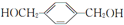 £¬ĘäĖłŗ¬¹ŁÄÜĶÅĆū³ĘĪŖōĒ»ł£®
£¬ĘäĖłŗ¬¹ŁÄÜĶÅĆū³ĘĪŖōĒ»ł£® £®
£®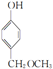 £¬
£¬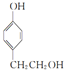 £¬
£¬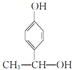 £¬
£¬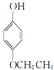 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ś¢Ł¢Ü¢Ū | B£® | ¢Ś¢Ū¢Ü¢Ł | C£® | ¢Ū¢Ü¢Ł¢Ś | D£® | ¢Ł¢Ü¢Ū¢Ś |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¾”ĮæŹ¹ÓĆ»ÆŹÆČ¼ĮĻ | B£® | ¾”Į¦·¢Õ¹Ēå½ąÄÜŌ“ | ||
| C£® | Ōö¼Ó¹¤³§ŃĢ“Ńøß¶Č | D£® | Ņ¹¼äÅŷŹ¤Ņµ·ĻĘų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬11.2LC5H12ŗ¬ÓŠµÄ·Ö×ÓŹżĪŖ0.5NA | |
| B£® | 21gŅŅĻ©Óė¶”Ļ©µÄ»ģŗĻĘųĢåÖŠŗ¬ÓŠ3NAøöC-H¼ü | |
| C£® | 1L0.1mol/LNH4NO3ČÜŅŗÖŠŗ¬ÓŠ0.2NAøöN | |
| D£® | ¹āÕÕĻĀ£¬1molCl2Óė×ćĮæCH4ĶźČ«·“Ó¦£¬Éś³ÉNAøöHCl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1.7æĖ-OHÖŠŗ¬ÓŠµÄµē×ÓŹżĪŖNA | |
| B£® | 42gŅŅĻ©Óė±ūĻ©µÄ»ģŗĻĘųĢåÖŠŗ¬Ģ¼Ō×ÓŹżĪŖ3NA | |
| C£® | ¶žĀČŅŅĻ©µÄ½į¹¹¼ņŹ½£ŗCH2=C£ØCl£©2 | |
| D£® | ŅŅĻ©ŗĶŅŅ“¼µÄ»ģŗĻĪļ¹²0.1mol£¬ĶźČ«Č¼ÉÕĖłĻūŗĵÄŃõĘųµÄ·Ö×ÓŹżŅ»¶ØĪŖ0.6 NA |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com