
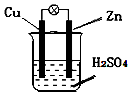
| A. | 负极发生的反应是:2H++2e-=H2↑ | |
| B. | 溶液中SO42-向铜片的方向移动 | |
| C. | 该装置实现了化学能转化为电能 | |
| D. | 若生成0.2mol H2,则有6.5克锌被还原 |
分析 锌铜原电池依据装置图分析,锌做负极失电子发生氧化反应生成锌离子,铜做正极,溶液中氢离子得到电子生成氢气,发生还原反应,电子流向从负极沿导线流向正极,溶液中阳离子移向正极.
解答 解:锌铜原电池依据装置图分析,锌做负极失电子发生氧化反应生成锌离子,铜做正极,溶液中氢离子得到电子生成氢气,发生还原反应,电子流向从负极沿导线流向正极,溶液中阳离子移向正极;
A、负极发生的反应是锌做负极失电子发生氧化反应生成锌离子,Zn-2e-=Zn2+,故A错误;
B、原电池中阴离子移向负极,溶液中SO42-向锌电极方向移动,故B错误;
C、电子由负极移向正极,电子由锌片通过导线流向铜,该装置实现了化学能转化为电能,故C正确;
D、若生成0.2mol H2,正极电极反应2H++2e-=H2↑,负极电极反应Zn-2e-=Zn2+,电子守恒得到,
H2~Zn~2e-
1 1 2
0.2mol 0.2mol
则锌被还原质量=65g/L×0.2mol=13g,故D错误;
故选C.
点评 本题考查了原电池原理的分析应用主要是电极反应、电极判断、能量变化和电子守恒的计算,掌握基础是关键,题目较简单.


科目:高中化学 来源: 题型:填空题
 ;其与NaHCO3溶液反应的化学反应方程式为
;其与NaHCO3溶液反应的化学反应方程式为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg+O2$\stackrel{△}{→}$MgO2 | B. | 2KClO3$→_{△}^{MnO_{2}}$2KCl+O2↑ | ||
| C. | 2NaOH+SO2→Na2SO4+H2O | D. | BaCl2+Na2CO3→BaCO3↓+2NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

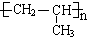 .
. .C中官能团的名称羰基、醛基.
.C中官能团的名称羰基、醛基.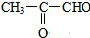 +2H2O.
+2H2O.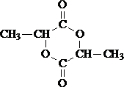 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、Y的浓度不再变化 | |
| B. | 单位时间生成amolX,同时生成3amolY | |
| C. | X、Y、Z的分子数之比为1:3:2 | |
| D. | X占混合气体的体积分数不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所得溶液的体积为22.5L | |
| B. | 该溶液物质的量浓度为10.00mol•L-1 | |
| C. | 根据题中数据,无法求得该溶液物质的量浓度 | |
| D. | 该溶液中溶质的质量分数因溶液的密度未知而无法求得 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com