
| A£® | ĄūÓĆCO2ŗĻ³É¾ŪĢ¼Ėįõ„æɽµ½āĖÜĮĻ£¬ŹµĻÖ”°Ģ¼”±µÄŃ»·ĄūÓĆ | |
| B£® | ĀČĖ®ÖŠ¼ÓČėĻ”ĮņĖį£¬æÉŌöĒæĀČĖ®µÄĘư׊Ō | |
| C£® | ÓĆÕŗÓŠÅØ°±Ė®µÄ²£Į§°ō¼ģŃéŹäĖĶĀČĘųµÄ¹ÜµĄŹĒ·ńĀ©Ęų | |
| D£® | ¼Ó¹¤ŗó¾ßÓŠĪüĖ®ŠŌµÄÖ²ĪļĻĖĪ¬æÉÓĆ×÷Ź³Ę·øÉŌļ¼Į |
·ÖĪö A£®ĄūÓĆCO2ŗĻ³É¾ŪĢ¼Ėįõ„Ąąæɽµ½āĖÜĮĻ£¬¼õÉŁ¶žŃõ»ÆĢ¼µÄÅÅ·Å£»
B£®ĀČĖ®ÖŠ“ęŌŚCl2+H2O?H++Cl-+HClO£¬øł¾ŻĘ½ŗāŅʶÆÅŠ¶Ļ£»
C£®NH3ÄÜÓėCl2·“Ӧɜ³ÉNH4Cl£¬øĆĪļÖŹŹĒŅ»ÖÖ°×É«¹ĢĢåĪļÖŹ£»
D£®¾ßÓŠĪüĖ®ŠŌµÄÖ²ĪļĻĖĪ¬ĪŽ¶¾£®
½ā“š ½ā£ŗA£®ĄūÓĆCO2ŗĻ³É¾ŪĢ¼Ėįõ„Ąąæɽµ½āĖÜĮĻ£¬ŹµĻÖ”°Ģ¼”±µÄŃ»·ĄūÓĆÓ¦ÓĆ£¬¼õÉŁ¶žŃõ»ÆĢ¼µÄÅÅ·Å£¬·ūŗĻĢāŅā£¬¹ŹAÕżČ·£»
B£®ĀČĖ®ÖŠ“ęŌŚCl2+H2O?H++Cl-+HClO£¬ĀČĖ®ÖŠ¼ÓČėĻ”ĮņĖį£¬ĒāĄė×ÓÅضČŌö“ó£¬Ę½ŗāĻņ×óŅĘ¶Æ£¬“ĪĀČĖįµÄÅØ¶Č¼õŠ”£¬ĀČĖ®µÄĘư׊Ō¼õČõ£¬¹ŹB“ķĪó£»
C£®NH3ŹĒ¼īŠŌĘųĢ壬æÉŅŌÓėCl2·“Ӧɜ³ÉNH4Cl£¬øĆĪļÖŹŹĒŅ»ÖÖ°×É«¹ĢĢåĪļÖŹ£¬æÉøł¾ŻŹĒ·ńĆ°°×ŃĢÓĆÅØ°±Ė®¼ģŃéŹäĖĶĀČĘųµÄ¹ÜµĄŹĒ·ńÓŠŠ¹Ā©£¬¹ŹCÕżČ·£»
D£®¾ßÓŠĪüĖ®ŠŌµÄÖ²ĪļĻĖĪ¬ĪŽ¶¾£¬ŌņæÉÓĆ×÷Ź³Ę·øÉŌļ¼Į£¬¹ŹDÕżČ·£®
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»ÆѧÓėÉś»ī”¢Éē»įĆÜĒŠĻą¹ŲÖŖŹ¶£¬Ö÷ŅŖæ¼²é°×É«ĪŪČ¾”¢ĀČĖ®µÄĘư׊Ō”¢°±ĘųµÄ»ÆѧŠŌ֏ѧµČÖŖŹ¶£¬ÕĘĪÕĪļÖŹµÄŠŌÖŹŗĶÓĆĶ¾ŹĒ¹Ų¼ü£¬ĢāÄæÄŃ¶Č²»“ó£®


 ŗ£µķ»ĘøŌĆūŹ¦µ¼ŗ½ĻµĮŠ“š°ø
ŗ£µķ»ĘøŌĆūŹ¦µ¼ŗ½ĻµĮŠ“š°ø ĘÕĶØøßÖŠĶ¬²½Į·Ļ°²įĻµĮŠ“š°ø
ĘÕĶØøßÖŠĶ¬²½Į·Ļ°²įĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
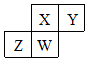 ¶ĢÖÜĘŚŌŖĖŲX”¢Y”¢Z”¢WŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĻą¶ŌĪ»ÖĆČē±ķĖłŹ¾£¬WŌ×ÓµÄÖŹ×ÓŹżŹĒĘä×īĶā²ćµē×ÓŹżµÄČż±¶£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
¶ĢÖÜĘŚŌŖĖŲX”¢Y”¢Z”¢WŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĻą¶ŌĪ»ÖĆČē±ķĖłŹ¾£¬WŌ×ÓµÄÖŹ×ÓŹżŹĒĘä×īĶā²ćµē×ÓŹżµÄČż±¶£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | ŌŖĖŲYÓŠĶ¬ĖŲŅģŠĪĢå | |
| B£® | ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄĖįŠŌ£ŗX£¾Z | |
| C£® | ¼ņµ„ĘųĢ¬Ēā»ÆĪļµÄČČĪČ¶ØŠŌ£ŗY£¾Z | |
| D£® | ŌÓŚ°ė¾¶£ŗW£¾Z£¾Y£¾X |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¹čĖįÄʵÄĖ®ČÜŅŗĖ׳ĘĖ®²£Į§£¬æÉÓĆ×÷ľ²Ä·Ą»š¼Į | |
| B£® | ”°µŲ¹µÓĶ”±½ūÖ¹Ź³ÓĆ£¬µ«æÉŅŌÓĆĄ“ÖĘ·ŹŌķ | |
| C£® | ÓĆ¾ŪŅŅĻ©ĖÜĮĻ“śĢę¾ŪČéĖįĖÜĮĻæɼõÉŁ°×É«ĪŪČ¾ | |
| D£® | ĄūÓĆĮøŹ³Äš¾Ę¾¹żĮĖµķ·Ū”śĘĻĢĒĢĒ”śŅŅ“¼µÄ»Æѧ±ä»Æ¹ż³Ģ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ļņµ°°×ÖŹČÜŅŗÖŠ¼ÓČėÅØĀČ»ÆĢśČÜŅŗ | |
| B£® | Į½ÖÖ²»Ķ¬Ę·ÅʵÄÄ«Ė®»ģŗĻ | |
| C£® | Ļņ±„ŗĶBaSO4ČÜŅŗÖŠ¼ÓČėÅØBaCl2ČÜŅŗ | |
| D£® | Ļņ±„ŗĶNa2CO3ČÜŅŗÖŠĶØČėCO2ĘųĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
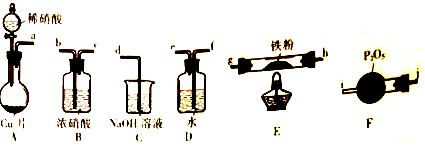
| A£® | ĮņĖįĶČÜŅŗĪüŹÕH2S£ŗCu2++S2-ØTCuS”ż | |
| B£® | “ÅŠŌŃõ»ÆĢśČÜÓŚĒāµāĖį£ŗFe3O4+8H+ØTFe2++2Fe3++4H2O | |
| C£® | Ļņ±„ŗĶĢ¼ĖįÄĘČÜŅŗÖŠĶØČė×ćĮæCO2£ŗCO32-+CO2+H2OØT2HCO3- | |
| D£® | ĻņKAl£ØSO4£©2ČÜŅŗÖŠ¼ÓČė¹żĮæµÄBa£ØOH£©2ČÜŅŗ£ŗAl3++2SO42-+2Ba2++4OH-ØT2BaSO4”ż+AlO2-+2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
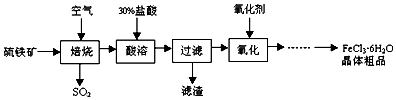
| A£® | ”°±ŗÉÕ”±·“Ó¦ÖŠ£¬Ńõ»Æ²śĪļŹĒSO2£¬»¹Ō²śĪļŹĒFe3O4 | |
| B£® | ”°ĖįČÜ”±Ź±µÄĖįæÉŅŌÓĆĻ”ĮņĖį“śĢę | |
| C£® | ”°¹żĀĖ”°ŗóµÄĀĖŅŗÖŠFe3+ŗĶFe2+µÄÅØ¶Č±ČĪŖ2£ŗ1 | |
| D£® | ”°Ńõ»Æ”±Ź±µÄŃõ»Æ¼ĮÖ»ÄÜєȔCl2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | x=0.3a£¬2Fe2++Cl2”ś2Fe3++2Cl- | |
| B£® | x=0.7a£¬2Br-+Cl2”śBr2+2Cl- | |
| C£® | x=1.2a£¬2Fe2++2Br-+2Cl2”śBr2+2Fe3++4Cl- | |
| D£® | x=1.5a£¬2Fe2++4Br-+3Cl2”ś2Br2+2Fe3++6Cl- |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com