

| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
分析 由浸出液中的金属阳离子主要是Mn2+,可知浸出时主要发生反应:SO2+MnO2═MnSO4,浸出液中含有少量的Fe2+、Al3+等,由离子开始沉淀及沉淀完全的pH可知,加入二氧化锰氧化过程,是将亚铁离子转化为铁离子,再加入石灰乳,调节溶液pH值,使铁离子、铝离子转化为氢氧化铁、氢氧化铝沉淀,再进行过滤,滤渣中主要有氢氧化铝、氢氧化铝,滤液为硫酸锰溶液,再通过蒸发浓缩、降温结晶,最后过滤得到硫酸锰晶体.
(1)二氧化锰与二氧化硫反应生成硫酸锰;
(2)由于二氧化硫溶于水生成H2SO3,H2SO3部分电离会使浸出液pH<2;
(3)加入二氧化锰氧化过程,是将亚铁离子转化为铁离子,自身被还原为锰离子,同时生成水;替代二氧化锰的试剂应具有强氧化性,且不能引入杂化;
(4)铁离子、铝离子水解程度比锰离子大,加热碳酸锰或氢氧化锰与氢离子反应,促进铁离子、铝离子水解;
(5)滤渣中主要有氢氧化铝、氢氧化铝,应将滤渣溶于足量的氢氧化钠溶液中,除去氢氧化铝,再进行过滤、洗涤、干燥,最后灼烧可得氧化铁.
解答 解:由浸出液中的金属阳离子主要是Mn2+,可知浸出时主要发生反应:SO2+MnO2═MnSO4,由于二氧化硫溶于水生成H2SO3,H2SO3部分电离会使浸出液pH<2,浸出液中含有少量的Fe2+、Al3+等,由离子开始沉淀及沉淀完全的pH可知,加入二氧化锰氧化过程,是将亚铁离子转化为铁离子,再加入石灰乳,调节溶液pH值,使铁离子、铝离子转化为氢氧化铁、氢氧化铝沉淀,再进行过滤,滤渣中主要有氢氧化铝、氢氧化铝,滤液为硫酸锰溶液,再通过蒸发浓缩、降温结晶,最后过滤得到硫酸锰晶体.
(1)由上述分析可知,二氧化锰与二氧化硫反应的化学方程式为:SO2+MnO2═MnSO4,
故答案为:SO2+MnO2═MnSO4;
(2)二氧化硫溶于水发生反应:SO2+H2O=H2SO3,生成的H2SO3部分电离:H2SO3?H++HSO3-,使浸出液的pH<2,
故答案为:二氧化硫溶于水发生反应:SO2+H2O=H2SO3,生成的H2SO3部分电离:H2SO3?H++HSO3-;
(3)加入二氧化锰氧化过程,是将亚铁离子转化为铁离子,反应离子方程式为:MnO2+2Fe2++4H+═Mn2++2Fe3++2H2O;
由表中数据可知,pH=9.7时Fe2+才完全沉淀,而pH=8.3时Mn2+已经开始沉淀,不能能取消“加入二氧化锰”的步骤;
替代二氧化锰的试剂应具有强氧化性,且不能引入杂化,氯气、酸性高锰酸钾、次氯酸均会引入杂质离子,而双氧水可以氧化亚铁离子为铁离子,同时生成水,不引入杂质离子,故选A;
故答案为:MnO2+2Fe2++4H+═Mn2++2Fe3++2H2O; 不能,pH=9.7时Fe2+才完全沉淀,而pH=8.3时Mn2+已经开始沉淀;A;
(4)铁离子、铝离子水解程度比锰离子大,加热碳酸锰或氢氧化锰与氢离子反应,促进铁离子、铝离子水解,进而转化为沉淀,再通过过滤除去,同意该同学的观点,
故答案为:同意,铁离子、铝离子水解程度比锰离子大,加热碳酸锰或氢氧化锰与氢离子反应,促进铁离子、铝离子水解,进而转化为沉淀,再通过过滤除去;
(5)从含硫酸锰的滤液中提取硫酸锰晶体的操作是:蒸发浓缩、降温结晶、过滤;
滤渣中主要有氢氧化铝、氢氧化铝,提取高纯度的铁红的方案为:将滤渣溶于足量的氢氧化钠溶液中,再进行过滤、洗涤、干燥,最后灼烧可得氧化铁.
故答案为:蒸发浓缩、降温结晶;过滤;将滤渣溶于足量的氢氧化钠溶液中,再进行过滤、洗涤、干燥,最后灼烧可得氧化铁.
点评 本题考查化学工艺流程、物质的分离提纯、对实验操作的分析评价、对数据的分析运用、实验方案设计等,是对学生综合能力的考查,难度中等.


科目:高中化学 来源: 题型:解答题
 与
与 D.乙烯与1-丁烯 E、乙烷与2,3-二甲基丁烷
D.乙烯与1-丁烯 E、乙烷与2,3-二甲基丁烷查看答案和解析>>
科目:高中化学 来源: 题型:解答题
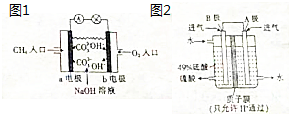 碳和硫的化合物在生产和生活中的应用非常广泛,清洁能源的开发、煤的综合利用等是实验“低碳生活”、减少空气污染的重要途径,试运用所学知识,回答下列问题:
碳和硫的化合物在生产和生活中的应用非常广泛,清洁能源的开发、煤的综合利用等是实验“低碳生活”、减少空气污染的重要途径,试运用所学知识,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 苯甲酸乙酯(C9H10O2)稍有水果气味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体、溶剂等.其制备方法为:
苯甲酸乙酯(C9H10O2)稍有水果气味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体、溶剂等.其制备方法为: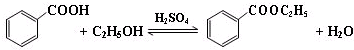
| 颜色、状态 | 沸点(℃) | 密度(g•cm-3) | |
苯甲酸* | 无色、片状晶体 | 249 | 1.2659 |
| 苯甲酸乙酯 | 无色澄清液体 | 212.6 | 1.05 |
| 乙醇 | 无色澄清液体 | 78.3 | 0.7893 |
| 环己烷 | 无色澄清液体 | 80.8 | 0.7318 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| A | ||
| B | C | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com