
【题目】ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。实验室中可通过以下反应制得:2KClO3+H2C2O4+H2SO4![]() 2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法不正确的是( )
2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法不正确的是( )
A.CO2是氧化产物
B.H2C2O4在反应中被氧化
C.H2C2O4的氧化性强于ClO2的氧化性
D.ClO2作水处理剂时,利用了其强氧化性
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】前四周期的A、B、C、D四种元素在周期表中均与元素X紧密相邻.已知元素X最高价氧化物的化学式为X2O5,B、D同主族且B元素的原子半径是同族元素中最小的,C的最高价氧化物对应的水化物是强酸.
(1)D元素基态原子的价电子排布式为______.
(2)B、X、D氢化物的沸点由高到低的顺序为______(用相应的化学式作答).
(3)E元素是A元素所在周期中电负性最大的,则EO3-的立体构型为______.
(4)F元素基态原子M层上有5对成对电子,F元素的名称为______.F形成的单质有δ、γ、α三种同素异形体,三种晶胞(如图所示)中F原子的配位数之比为______,δ、γ、α三种晶胞的密度之比为______.

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂用废铜铁合金制取生产油漆的颜料铁红(Fe2O3),并回收铜的流程如下:
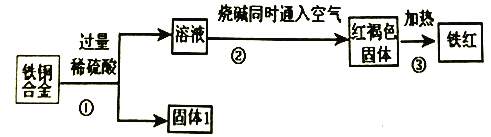
完成下列问题:
(1)上述三个过程中发生了氧化还原反应的是____________(填符号①②③)。
(2)固体1的名称______;红褐色固体的化学式______ 。
(3)写出整个②过程发生反应的离子方程式:______ ;______ ;______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢溴酸在医药和石化工业上有广泛用途。如图所示是模拟工业制备氢溴酸粗产品并精制的流程:

根据上述流程回答下列问题:
(1)混合①中发生反应的离子方程式为_______________________________。
(2)混合①中使用冰水的目的是______________________________________。
(3)混合②中加入Na2SO3的目的是____________________________________________。
(4)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸(工业氢溴酸)带有淡淡的黄色。于是甲乙两同学设计了简单实验进行探究:甲同学假设工业氢溴酸呈淡黄色是因为其中含有Fe3+,则用于证明该假设所用的试剂为______,若假设成立可观察到的现象为________________;乙同学假设工业氢溴酸呈淡黄色是因为其中含有______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某次实验需用480mL、0.5mol/L 的稀硫酸,某同学用98%的浓硫酸(ρ=1.84g/cm3) 进行配制,请回答下列问题:
(1) 实验需要的玻璃仪器除了烧杯,胶头滴管、量简、玻璃棒,还需要__________;
(2)计算: 需用量筒量取浓硫酸的体积为__________ mL;
(3) 配制过程:
①用量筒量取所需的浓硫酸
②将浓硫酸缓缓注入盛有适量蒸馏水的烧杯中,边加边搅拌,冷却至室温
③用玻璃棒引流将烧杯中的溶液转移到已经检漏的合适规格的容量瓶中
④洗涤烧杯和玻璃棒2~3 次,洗涤液也注入容量瓶中,轻轻摇动容量瓶,使溶液混合均匀
⑤向容量流中加入蒸馏水,在距离刻度1~2cm 时,然后定容
⑥盖好瓶塞,反复上下颠倒,摇匀;
⑦将配制好的溶液转移至试剂瓶中待用。
上述步骤中一定用到胶头滴管的有__________(填序号);
若步骤⑤定容时加水超过刻度线,应该如何处置:___________。
(4) 在横线上填写下列各种情况对所配制溶液浓度的影响(选填“偏高”、“偏低”或“无影响”).
①所用的浓硫酸长时间放置在密封不好的容器中______;
②用量简量取浓硫酸时仰视液面______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为部分短周期元素在元素周期表中的位置,回答下列问题
IA | IIA | IIIA | IVA | VA | VIA | VIIA | |
1 | ① | ||||||
2 | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)写出由①、④两种元素形成的既含极性键又含非极性键的一种化合物的化学式______;
由①、③、⑧三种元素形成的一种离子化合物的电子式_______________。
(2)工业上制备元素⑥单质的方程式为_________________________________。
(3)①、②两种元素形成的离子化合物中,两种简单离子的半径大小_____________(用微粒符号表示);用一个化学反应方程式表示元素⑧的非金属性强于元素⑦_________________。
(4)常温下,将元素⑧的单质通入⑤的最高价氧化物的水溶液中,两者恰好反应,此时溶液中离子浓度由大到小的顺序是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当三份Cu粉分别与过量的稀硝酸、浓硝酸、热的浓硫酸反应后,收集到的气体在相同状况下体积相等时,三份Cu粉的质量比为(不考虑NO2转化为N2O4和反应生成气体的溶解)( )
A. 3∶1∶2 B. 3∶2∶2
C. 1∶1∶2 D. 2∶6∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用石油的裂解气与煤的气化产品合成有机物H,A在标准状况下的密度为1. 25 g L-1,B是天然气的主要成分,H是有香味的油状液体。

请回答:
(1)有机物A的官能团名称为________。
(2)③的反应类型是________。
(3)写出②的化学方程式: ________。
(4)下列说法不正确的是________。
A.有机物C是工业酒精中含有的成分且有毒
B.有机物H可用来制肥皂
C.鉴别有机物C、H和CH3COOH可用新制Cu(OH)2悬浊液
D.有机物H中混有CH3COOH与有机物C,可用饱和Na2CO3溶液提纯H
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 绿色植物的光合作用是把热能转化为化学能的过程
B. 生物能是与化学反应无关的一种能源
C. 化学能只能以热能的形式释放
D. 葡萄糖在人体内的氧化是放热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com