
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®³£ĪĀĻĀ£¬ĪļÖŹµÄĮæÅØ¶Č¾łĪŖ0.1mol”¤L?1Na2CO3ŗĶNaHCO3µÄµČĢå»ż»ģŗĻČÜŅŗÖŠ£ŗ
2c(OH?)£2c(H+)£½3c(H2CO3)£«c(HCO3£)£c(CO32?)
B£®¦¤H£¼0,¦¤S£¾0µÄ·“Ó¦¶¼ŹĒ×Ō·¢·“Ó¦£¬¦¤H£¾0,¦¤S£¾0µÄ·“Ó¦ČĪŗĪĢõ¼ž¶¼ŹĒ·Ē×Ō·¢·“Ó¦£»
C£®ŅŃÖŖ£ŗP4(g)£«6Cl2(g)£½4PCl3(g) ¦¤H£½akJ”¤mol£1?
P4(g)£«10Cl2(g)£½4PCl5(g)¦¤H£½ bkJ”¤mol£1
P4¾ßÓŠÕżĖÄĆęĢå½į¹¹£¬PCl5ÖŠP£Cl¼üµÄ¼üÄÜĪŖckJ”¤mol£1,PCl3ÖŠP£Cl¼üµÄ¼üÄÜĪŖ1.2ckJ”¤mol£1£¬ÓÉ“Ė¼ĘĖćCl£Cl¼üµÄ¼üÄÜ

D£®ŌŚŅ»¶ØĪĀ¶ČĻĀ£¬¹Ģ¶ØĢå»żĪŖ2LĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦£ŗ2SO2(g)+O2(g) 2SO3(g)
2SO3(g)
”÷H£¼0£¬µ±v(SO2)= v(SO3)Ź±£¬ĖµĆ÷øĆ·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬
A
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗA”¢øł¾ŻÖŹ×ÓŹŲŗć£¬¶ŌÓŚNa2CO3ČÜŅŗ£ŗc(OH?)=c(H+)+2c(H2CO3)£«c(HCO3£)£»¶ŌÓŚNaHCO3ČÜŅŗ£ŗc(OH?)+c(CO32?)£½c(H+)+c(H2CO3)£»Į½ÕßµČÅØ¶Č”¢µČĢå»ż»ģŗĻŗó£¬ČÜŅŗÖŠĮ½ÖÖČÜÖŹµÄĪļÖŹµÄĮæĻąµČ£¬ĖłŅŌ£¬½«ÉĻŹöĮ½Ź½µž¼Ó£ŗ[c(OH?)=c(H+)+2c(H2CO3)£«c(HCO3£)]+[ c(OH?)+c(CO32?)£½c(H+)+c(H2CO3)]£¬ŅĘĻī£¬¼“µĆ2c(OH?)£2c(H+)£½3c(H2CO3)£«c(HCO3£)£c(CO32?)£¬ÕżČ·£»B”¢¦¤H£¾0£¬¦¤S£¾0 ŌŚ½ĻøßĪĀ¶ČĻĀÄÜ×Ō·¢£¬“ķĪó£»C”¢½«Į½øö·“Ó¦Ź½·Ö±š±ąŗÅĪŖ¢ŁŗĶ¢Ś£¬(¢Ś - ¢Ł)”Ā4æÉµĆ£ŗPCl3(g)+Cl2(g)= PCl5(g) £»¦¤H£½ ”£ÓÉ£ŗ
”£ÓÉ£ŗ
PCl3(g)??? +??? Cl2(g)??? =????? PCl5(g)
¶Ļ1øöP£Cl¼ü?? ¶Ļ1øöCl£Cl¼ü?? ³É1øöP£Cl¼ü
3”Į1.2c???????? Q????????????? ??????????? 5”Įc
(3.6c + Q -5c)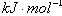 =
= £¬ Q=
£¬ Q= £¬¹ŹC“ķ”£
£¬¹ŹC“ķ”£
DŃ”Ļī£¬²»Ķ¬ĪļÖŹ±ķŹ¾ĖŁĀŹ£¬µ½“ļĘ½ŗāŹ±£¬ÕżÄęĖŁĀŹÖ®±ČµČÓŚ»Æѧ¼ĘĮæŹżÖ®±Č£¬Čē£¬VÕż£ØSO2£©£ŗVÄę£ØSO3£©= 2 : 2£¬¼“VÕż£ØSO2£©=VÄę£ØSO3£©”£¶ų¶Ōv(SO2)=v(SO3)Ī“ÖøĆ÷·“Ó¦ĖŁĀŹµÄ·½Ļņ£¬¹Ź“ķĪó£»
æ¼µć£ŗæ¼²é»Æѧ·“Ó¦ĖŁĀŹÓė»ÆŃ§Ę½ŗā£¬µē½āÖŹČÜŅŗµČ»ł±¾ĄķĀŪ


 »Ŗ¶«Ź¦“ó°ęŅ»æĪŅ»Į·ĻµĮŠ“š°ø
»Ŗ¶«Ź¦“ó°ęŅ»æĪŅ»Į·ĻµĮŠ“š°ø ĆĻ½ØĘ½ĆūŠ£æ¼¾ķĻµĮŠ“š°ø
ĆĻ½ØĘ½ĆūŠ£æ¼¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā

| ČŻĘ÷ | ¼× | ŅŅ | ±ū |
| ·“Ó¦ĪļĶ¶ČėĮæ | 1mol CH3OCH3”¢1mol H2O | 2mol CH3OH | 1mol CH3OH |
| CH3OHµÄÅØ¶Č£Ømol/L£© | c1 | c2 | c3 |
| ·“Ó¦µÄÄÜĮæ±ä»Æ | ĪüŹÕa kJ | ·Å³öb kJ | ·Å³öc kJ |
| Ę½ŗāŹ±Ģå»ż£ØL£© | V1 | V2 | V3 |
| ·“Ó¦Īļ×Ŗ»ÆĀŹ | ¦Į 1 | ¦Į 2 | ¦Į 3 |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
 ·Ē½šŹōŌŖĖŲµŖÓŠ¶ąÖÖŃõ»ÆĪļ£¬ČēNO”¢NO2”¢N2O4µČ£®
·Ē½šŹōŌŖĖŲµŖÓŠ¶ąÖÖŃõ»ÆĪļ£¬ČēNO”¢NO2”¢N2O4µČ£®| Ź±¼ä£Øs£© | 0 | 20 | 40 | 60 | 80 |
| n£ØNO2£©/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n£ØN2O4£©/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| ||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
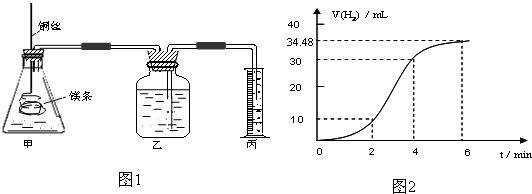
| ŹµŃ鱹ŗÅ | ¢ń | ¢ņ | ¢ó | ¢ō |
| 10%H2O2µÄĢå»ż/mL | 5.0 | 5.0 | V1 | V2 |
| 20%ĮņĖįµÄĢå»ż/mL | 0 | 0.5 | 1.0 | V3 |
| Ė®µÄĢå»ż/mL | 15 | 14.5 | V4 | 13.5 |
| ĖłŠčŹ±¼ät/s | t1 | t2 | t3 | t4 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com