
| A. | 1molO2与金属Na反应,O2一定得到4NA个电子 | |
| B. | 18g NH4+中所含的电子数为11NA | |
| C. | 1molFe与足量的Cl2反应,转移的电子数为2NA | |
| D. | 1molCl2与足量的Fe反应,转移的电子数为2NA |
分析 A.氧气和钠反应可以生成氧化钠,也可以过氧化钠;
B.一个NH4+中所含的电子数为10;
C.Cl2具有强氧化性Cl2,Fe→Fe3+,1molFe失去电子数为3NA;
D.Cl2→2Cl-,1molCl2得到的电子数为2NA.
解答 解:A.氧气和钠反应可以生成氧化钠,也可以生成过氧化钠,2mol O2与金属钠反应,反应生成氧化钠电子转移4mol,生成过氧化钠电子转移2mol,O2不一定得到4NA个电子,故A错误;
B.18g NH4+中含有NH4+的数目为$\frac{18g}{18g/mol}$×${N}_{A}mo{l}^{-1}$=NA,一个NH4+中所含的电子数为10,因此18g NH4+中所含的电子数为10NA,故B错误;
C.Cl2具有强氧化性Cl2,Fe→Fe3+,1molFe失去电子数为3NA,因此转移电子数为3NA,故C错误;
D.Cl2→2Cl-,1molCl2得到的电子数为1mol×${N}_{A}mo{l}^{-1}$×2=2NA,故D正确;
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大,注意掌握转移电子数的计算方法.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
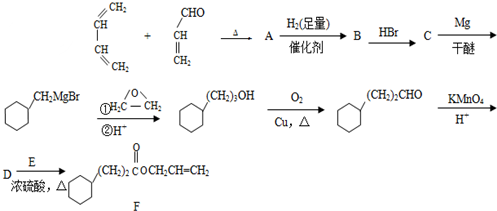

 ,A中所含官能团的名称是醛基、碳碳双键;
,A中所含官能团的名称是醛基、碳碳双键; ;
; ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量N2和CO2中,共用电子对的个数比为3:4 | |
| B. | 该反应中化合价变化的有N和C元素 | |
| C. | 氧化剂与还原剂的物质的量之比为1:1时,NOx中氮元素的化合价为+2价 | |
| D. | 当x=2时,每生成1mol N2,转移电子数为4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaNO2发生的是氧化反应 | B. | 生成1molN2时转移的电子数为3mol | ||
| C. | NH4Cl中的N元素被还原 | D. | N2既是氧化剂有事还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
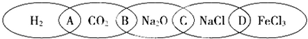
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
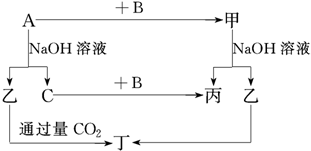
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 植树造林,加强绿化 | B. | 合理使用化肥和农药 | ||
| C. | 工业“三废”经处理后再排放 | D. | 矿物产品的综合开发和利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com