
【题目】下列叙述中,错误的是( )
A.同温同压下,气体的体积之比等于它们的物质的量之比
B.同温同压下,气体的体积之比等于它们的质量之比
C.同温同压下,相同体积的气体的质量之比等于它们的相对分子质量之比
D.同温同压下,气体的密度之比等于它们的相对分子质量之比
科目:高中化学 来源: 题型:
【题目】下列各组离子在强碱性溶液里能大量共存的是 ( )
A. Na+、K+ 、Mg2+、SO42- B. Ba2+ 、Na+ 、NO3-、HCO3-
C. Na+、K+ 、S2- 、CO32- D. Na+ 、S2- 、ClO- 、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝热反应不仅被应用于焊接钢轨,而且常应用于冶炼熔点较高的金属如钒、铬、锰等。这是利用了铝的①还原性 ②导电性 ③与强酸和强碱均反应 ④被氧化的过程放出大量的热
A. ① B. ①④ C. ①③④ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热N2O5依次发生的分解反应为:
①N2O5(g) ![]() N2O3(g)+O2(g)
N2O3(g)+O2(g)
②N2O3(g) ![]() N2O(g)+O2(g)
N2O(g)+O2(g)
在容积为2 L的密闭容器中充入8 mol N2O5,加热到t ℃,达到平衡状态后O2为9 mol,N2O3为3.4 mol。则平衡体系中N2O5的物质的量浓度为
A. 1.8mol/L B. 0.9 mol/L C. 2.3 mol/L D. 4.0 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 甲烷和乙烯均可使酸性KMnO4溶液褪色
B. 纤维素、淀粉和蛋白质都是高分子化合物
C. 煤的干馏和石油的分馏均属化学变化
D. 葡萄糖和淀粉均能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关碱金属元素,下列说法正确的是( )
A. 单质沸点随原子序数的递增而升高
B. 周期表第一列是第IA族元素,又称碱金属元素
C. 金属锂在空气中燃烧,产物是Li2O2
D. 金属锂常用于制造锂电池,这跟它还原性强、密度小有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解200mL的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.1mol碱式碳酸铜晶体(不含结晶水)后,恰好恢复到电解前的浓度(不考虑二氧化碳的溶解)。下列说法正确的是( )
A. 电解过程中转移的物质的量为0.2 mol B. 电解过程中共产生气体5.6L
C. 原溶液的物质的量浓度为1.0mol/L D. 电解过程中,阴极产物只有Cu单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气和水,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是__________________。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时:负极的电极反应式是_______________________________________ 。
(3)用CO做燃料电池电解CuSO4溶液、FeCl3和FeCl2混合液的示意图如图1所示,其中A、B、D均为石墨电极,C为铜电极.工作一段时间后,断开K,此时A、B两极上产生的气体体积相同.
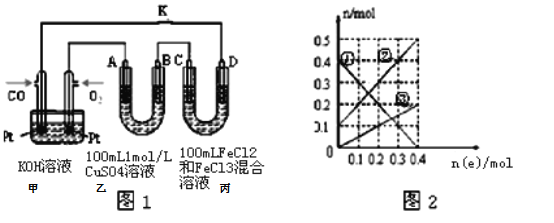
①写出通入CO的电极反应式____________________________________
②乙中B极产生的气体在标准状况下的体积为_____________.
③丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图2所示,则图中③线表示的是____________(填离子符号)的变化;反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要_____________mL 8.0mol·L﹣1 NaOH溶液。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com