
| 元素 | 有 关 信 息 |
| A | 元素主要化合价为-2,原子半径为0.074 nm |
| B | 所在主族序数与所在周期序数之差为4 |
| C | 原子半径为0.102 nm,其单质为黄色晶体,可在A的单质中燃烧 |
| D | 最高价氧化物的水化物能按1︰1电离出电子数相等的阴、阳离子 |
| E | 原子半径为0.075 nm,最高价氧化物的水化物可与其氢化物形成一种盐X |
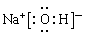 ;
; Cl-+ H+ + HClO ;
Cl-+ H+ + HClO ; NH3·H2O + H+ ;
NH3·H2O + H+ ;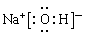 。(2)Cl2与水反应的两种方程式为:Cl2+H2O
。(2)Cl2与水反应的两种方程式为:Cl2+H2O H++Cl-+HClO。(3)元素O和Na形成的化合物Na2O2可作为呼吸面具中氧气的来源,该反应的化学方程式为2Na2O2 + 2CO2 ="=" 2Na2CO3 + O2。(4)X NH4NO3是强酸弱碱盐,在溶液中存在水解平衡:NH4++ H2O
H++Cl-+HClO。(3)元素O和Na形成的化合物Na2O2可作为呼吸面具中氧气的来源,该反应的化学方程式为2Na2O2 + 2CO2 ="=" 2Na2CO3 + O2。(4)X NH4NO3是强酸弱碱盐,在溶液中存在水解平衡:NH4++ H2O NH3·H2O + H+,消耗了水电离产生的OH-,使OH-的浓度减小,促进了水的电离,当最终达到电离平衡时,由于溶液中c(OH-)<c(H+).所以其水溶液显酸性。(5)O2的相对分子质量为32,与其等式量的N的氢化物的化学式为N2H4,俗称联氨。燃料N2H4与空气组成的燃料电池中,燃料N2H4为负极,空气的电极为正极。电解质溶液是30%的KOH溶液,则该电池放电时的正极电极反应式为O2+2H2O+4e- ="=" 4OH- 。(6)在整个闭合回路中电子转移的物质的量相等。若使用Y—空气燃料电池精炼铜,当得到精铜80 g时,n(Cu)=80g÷64g/mol=1.25mol,所以n(e-)=2.5mol.即燃料电池中转移的电子数N=2.5NA。
NH3·H2O + H+,消耗了水电离产生的OH-,使OH-的浓度减小,促进了水的电离,当最终达到电离平衡时,由于溶液中c(OH-)<c(H+).所以其水溶液显酸性。(5)O2的相对分子质量为32,与其等式量的N的氢化物的化学式为N2H4,俗称联氨。燃料N2H4与空气组成的燃料电池中,燃料N2H4为负极,空气的电极为正极。电解质溶液是30%的KOH溶液,则该电池放电时的正极电极反应式为O2+2H2O+4e- ="=" 4OH- 。(6)在整个闭合回路中电子转移的物质的量相等。若使用Y—空气燃料电池精炼铜,当得到精铜80 g时,n(Cu)=80g÷64g/mol=1.25mol,所以n(e-)=2.5mol.即燃料电池中转移的电子数N=2.5NA。

科目:高中化学 来源:不详 题型:单选题
| A.SO2、SO3都是极性分子 |
| B.在NH4+和[Cu(NH3)4]2+中都存在配位键 |
| C.元素电负性越大的原子,吸引电子的能力越强 |
| D.PCl3和NF3分子中所有原子的最外层都达到8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、+4、-2 | -2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 元素代号 | L | M | X | R | T |
| 原子半径(nm) | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
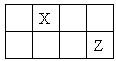
| A.原子半径: r(Y)> r (Z)> r (W) |
| B.Y、Z、W的简单离子的电子层结构相同 |
| C.XWm与YWn中化学键类型相同(m、n为正整数) |
| D.元素Z 的简单气态氢化物的热稳定性比W 的强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②④⑤ | B.①②④ | C.②③⑤ | D.全部正确 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
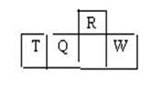
| A.最简单气态氢化物的热稳定性:R>Q |
| B.最高价氧化物对应水化物的酸性:Q<W |
| C.原子半径:T>Q>R |
| D.含T的盐溶液一定显酸性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.镭比钙的金属性更强 | B.在化合物中呈+2价 |
| C.镭是一种放射性元素 | D.氢氧化镭呈两性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com