

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����NaCl��Һ������ | B����NaCl��Һ��Kw=1��10-14 |
| C����NaCl��Һϡ��10����pH=7 | D����NaCl��Һ��Kw=1��10-12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������չ����Դ | B���������̫���� |
| C��ʹ�ú�̼��Դ | D�������Դ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ʼʱ����ʹ�����ҺPH��ͬ |
B��V(NaOH)=10��00 mL ʱ��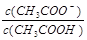 ��1 ��1 |
| C��pH=7ʱ������������NaOH��Һ�������ȣ������õ������ |
| D��V(NaOH)="20" ��00 mL ʱ��c(Cl?)��c(CH3COO��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��pH��0����Һ�������� | B��0.04 mol��L��1H2SO4 |
| C��0.5 mol��L��1HCl | D��0.05 mol��L��1CH3COOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| ��ѧ�� | H��H | Cl��Cl | H��Cl |
| ���� | 436 kJ��mol��1 | 243 kJ��mol��1 | 431 kJ��mol��1 |
 H2(g)��
H2(g)�� Cl2(g)=HCl(g)��H����91.5 kJ��mol��1
Cl2(g)=HCl(g)��H����91.5 kJ��mol��1 H2(g)��
H2(g)�� Cl2(g)=HCl(g)��H��91.5 kJ��mol��1
Cl2(g)=HCl(g)��H��91.5 kJ��mol��1�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��V3>V2>V1 | B��V3>V2=V1 |
| C��V3=V2>V1 | D��V1=V2>V3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�������з������л��ܼ����ˮ��Ϊ��ȡ�� |
| B����ǿ��ú��ʯ�͡���Ȼ�����ۺ����õ��о������ȼ�ϵ������� |
| C������CO2�ϳɾ�̼������ɽ������ϣ�ʵ�֡�̼����ѭ������ |
| D��������Ҵ���ȼ���ȷֱ���891��0 kJ��mol��1��1366��8 kJ��mol��1�����ü��������̼�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ʯȼ�����κ������¶��ܳ��ȼ�� |
| B����ʯȼ����ȼ�չ������ܲ�����Ⱦ������CO��SO2���к����� |
| C��ֱ��ȼ��ú���罫ú������ӹ���ȼ��Ч���� |
| D������ú��Ϊ����ȼ�Ϻ�,ȼ��Ч�ʽ����� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com