
| 选项 | 目的 | 分离方法 | 原理 |
| A | 使用CCl4提取碘水中的碘 | 萃取、分液 | 碘在CCl4中的溶解度较大 |
| B | 分离乙酸乙酯和乙醇 | 分液 | 乙酸乙酯和乙醇的密度不同 |
| C | 除去淀粉胶体中的NaCl | 过滤 | 淀粉胶体不能透过滤纸 |
| D | 分离氯化钠和氯化铵 | 升华 | 氯化铵易升华 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.碘不易溶于水,易溶于四氯化碳;
B.乙酸乙酯和乙醇互溶,不分层;
C.胶体、溶液均可透过滤纸;
D.氯化铵加热分解生成气体,遇冷化合生成氯化铵.
解答 解:A.碘不易溶于水,易溶于四氯化碳,则萃取、分液可分离,故A正确;
B.乙酸乙酯和乙醇互溶,不分层,不能利用分液法分离,故B错误;
C.胶体、溶液均可透过滤纸,不能利用过滤分离,应选渗析法,故C错误;
D.氯化铵加热分解生成气体,遇冷化合生成氯化铵,氯化铵不能升华,加热可分离,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、性质差异、混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意实验的评价性分析,题目难度不大.


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 20% | B. | 12.5% | C. | 17.5% | D. | 25% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.75 mol•L-1 | B. | 1.5 mol•L-1 | C. | 2 mol•L-1 | D. | 0.15 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑧ | B. | ③⑥⑨⑩ | C. | ④⑤⑧⑨ | D. | ④⑤⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
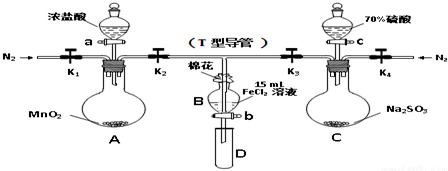
| 过程ⅣB溶液中含有的离子 | 过程ⅥB溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 弱电解质的导电能力一定比强电解质的导电能力弱 | |
| B. | pH=4的醋酸与pH=10的NaOH溶液等体积混合后溶液显碱性 | |
| C. | 豆浆中加入硫酸钙会使蛋白质聚沉. | |
| D. | 同浓度的①NaHCO3②Na2CO3③CH3COONa四种溶液,pH值大小排列顺序是②>①>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质发生化学反应都伴随着能量变化 | |
| B. | 伴有能量变化的物质变化不一定都是化学反应 | |
| C. | 在一个确定的化学反应关系中,反应物的总能量与生成物的总能量一定不同 | |
| D. | 在一个确定的化学反应关系中,反应物的总能量总是大于生成物的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
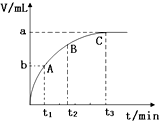 为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.
为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.| 编号 | 操 作 | 实验现象 |
| ① | 分别在试管A、B中加入 5mL 5% H2O2溶液,各滴入1~2 滴1mol/L FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中;将试管B放入盛有40℃左右热水的烧杯中. | 试管A中不再产生气泡,试管B中产生的气泡量增大 |
| ② | 另取两支试管分别加入 5mL 5%H2O2溶液和 5mL10%H2O2溶液. | 试管A、B中均未见气泡产生 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com