
分析 【实验一】取一定量制得的氢氧化铜固体,于坩埚中灼烧,当温度达到80~100℃得到黑色固体粉末,继续加热至1000℃以上,黑色粉末全部变成红色粉末氧化亚铜,说明高温时,+1价的铜比+2价的铜稳定,取适量红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸(或盐酸),Cu2O+2H+=Cu2++Cu+H2O得到蓝色溶液,同时观察到试管底部还有红色固体存在,说明溶液中,+2价的铜比+1价的铜稳定.
(1)根据信息:氢氧化铜固体,于坩埚中灼烧,当温度达到80~100℃得到黑色固体粉末为氧化铜;继续加热至1000℃以上,黑色粉末全部变成红色粉末氧化亚铜,说明高温+1价铜稳定;
(2)根据信息:红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液为+2价的铜盐溶液,同时观察到试管底部还有红色固体存在为铜单质,据此书写化学方程式;
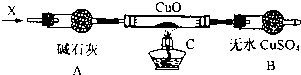
【实验二】将X通入灼热的CuO燃烧管完全反应后,生成物中还有一种能使澄清石灰水变浑浊的气体Y应为二氧化碳,消耗0.01mol X,无水硫酸铜变成蓝色,测得B装置增重0.54g,即生成水0.03mol,并收集到0.88g气体Y即0.02molCO2,根据碳元素和氢元素守恒可知,某种气态烃(X)为C2H6,
(3)根据原子守恒确定气态氢化物的化学式,计算摩尔质量;
(4)根据实验现象来书写化学方程式.
解答 解:【实验一】问题1:铁和铜都有变价,具有相似点,正二价铁的稳定性小于正三价的铁,探究正一价铜的稳定性是否也小于正二价的铜,解决问题取一定量制得的氢氧化铜固体,于坩埚中灼烧,当温度达到80~100℃得到黑色固体粉末,继续加热至1000℃以上,黑色粉末全部变成红色粉末氧化亚铜,说明高温时,+1价的铜比+2价的铜稳定,取适量红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸(或盐酸),Cu2O+2H+=Cu2++Cu+H2O得到蓝色溶液,同时观察到试管底部还有红色固体存在,说明溶液中,+2价的铜比+1价的铜稳定.
(1)根据信息:氢氧化铜固体,于坩埚中灼烧,当温度达到80~100℃得到黑色固体粉末;继续加热至1000℃以上,黑色粉末全部变成红色粉末氧化亚铜,根据在不同温度下反应物的组成可确定物质的稳定性,所以高于1000℃时Cu2O比CuO稳定,在溶液中:Cu2O+2H+=Cu+Cu2++H2O,所以Cu2+比Cu+稳定,
故答案为:高温时,+1价的铜比+2价的铜稳定,而溶液中,+2价的铜比+1价的铜稳定;
(2)根据信息:红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液为+2价的铜盐溶液,同时观察到试管底部还有红色固体为铜单质,Cu2O中+1价的铜在酸性溶液中发生氧化还原反应:Cu2O+2H+=Cu+Cu2++H2O,
故答案为:Cu2O+2H+=Cu+Cu2++H2O;
【实验二】将X通入灼热的CuO燃烧管完全反应后,生成物中还有一种能使澄清石灰水变浑浊的气体Y应为二氧化碳,消耗0.01mol X,无水硫酸铜变成蓝色,测得B装置增重0.54g,即生成水0.03mol,并收集到0.88g气体Y即0.02molCO2,根据碳元素和氢元素守恒可知,某种气态烃(X)为C2H6,
(3)根据上面的分析可知,X为C2H6,X气体其摩尔质量为30g/mol,
故答案为:30g/mol;
(4)C中发生反应的化学方程式为C2H6和氧化铜反应:7CuO+C2H6$\frac{\underline{\;\;△\;\;}}{\;}$7Cu+2CO2↑+3H2O,
故答案为:7CuO+C2H6$\frac{\underline{\;\;△\;\;}}{\;}$7Cu+2CO2↑+3H2O.
点评 本题考查实验探究和数据处理,做题时注意变价金属氧化物的性质以及质量守恒定律计算物质的化学式.题目难度中等.


科目:高中化学 来源: 题型:选择题
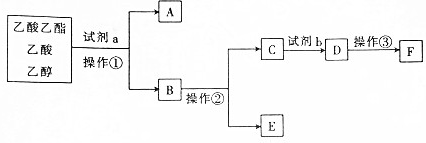
| A. | 操作②是蒸馏 | |
| B. | 试剂a可能是饱和碳酸钠溶液 | |
| C. | 试剂b比同浓度的D溶液酸性强 | |
| D. | A与E在浓硫酸加热的条件下可生成乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四种元素均可与氢元素形成 18电子分子 | |
| B. | X、Y、Z、W形成的单质最多有 6种 | |
| C. | 四种元素中,Z的最高价氧化物对应水化物酸性最强 | |
| D. | 四种元素的原子半径:rZ>rX>rY>rW |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 雾霾是一种分散系,分散剂是空气,带活性炭口罩防雾霾的原理是吸附原理 | |
| B. | 聚乙炔用I2或Na等做掺杂处理后可形成一种导电塑料,该导电塑料是一种纯净物 | |
| C. | 用蘸有浓氨水的棉棒检验输送氯气的管道是否漏气 | |
| D. | 用合成聚碳酸酯可降解塑料,实现“碳”的循环利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
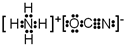 或
或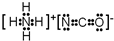 .
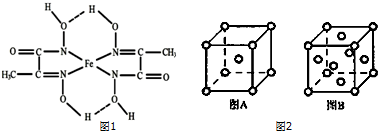
.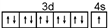 .A、B元素形成的最简单的化合物不能与E2+形成配合物的原因是CH4不能提供孤对电子.
.A、B元素形成的最简单的化合物不能与E2+形成配合物的原因是CH4不能提供孤对电子.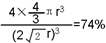 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 外围电子就是最外层电子 | |
| B. | 最外层电子数小于4的元素一定是金属元素 | |
| C. | 过渡元素的最外层电子数一般为1个或2个 | |
| D. | 如果某元素最外层电子数是1个或2个,次外层电子数为18个,此元素是副族元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油分馏时把温度计插入液面下 | |
| B. | 向银氨溶液中加入几滴乙醛后用酒精灯加热至沸腾制银镜 | |
| C. | 检验卤代烷中的卤素元素可先将卤代烷与NaOH溶液混合加热,然后加入AgNO3溶液,根据生成沉淀的颜色初步确定卤素 | |
| D. | 用乙醇、醋酸和18mol/L的硫酸混合加热制乙酸乙酯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com