
����Ŀ�����̿�(��Ҫ�ɷ�MnO2�����ʽ���Ԫ��Fe��Al��Mg��)��ˮ����Һ��������SO2��Ӧ���Ʊ�MnSO4��H2O ����Ӧ�Ļ�ѧ����ʽΪ��MnO2��SO2=MnSO4
��1������Ϊ17��40g����MnO2���������_____L(��״��)SO2��
��2����֪��Ksp[Al(OH)3]=1��10��33��Ksp[Fe(OH)3]=3��10��39��pH=7��1ʱMn(OH)2��ʼ�����������£���ȥMnSO4��Һ�е�Fe3����Al3��(ʹ��Ũ��С��1��10��6mol��L��1)���������ҺpH��ΧΪ________��
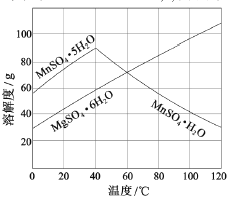
��3����ͼ���Կ�������MnSO4��MgSO4�����Һ�нᾧMnSO4��H2O���壬��
���ƽᾧ�¶ȷ�ΧΪ_______��
��4��ȷ��ȡ0��1710gMnSO4��H2O��Ʒ������ƿ�У���������H2PO4��NH4NO3��Һ������ʹMn2��ȫ��������Mn3������c(Fe2��)=0��0500mol��L��1�ı���Һ�ζ����յ�(�ζ�������Mn3������ԭΪMn2��)������Fe2����Һ20��00mL������MnSO4��H2O��Ʒ�Ĵ���(������������)
���𰸡���1��4��48����2��5��0<pH<7��1����3������60�棻��4������������ԭ��Ӧ�е�ʧ�����غ㣺n(Mn3��)��1=n(Fe2��)��1=20��00��10��3��0��0500mol=1��00��10��3mol������MnԪ���غ㣬m��MnSO4��H2O��=1��00��10��3��169g=0��169g�������ǣ�0��169/0��1710��100%=98��8%��
����������1�����ݷ�Ӧ����ʽ��n(SO2)=n(MnO2)=17��4/87mol=0��2mol����0��2��22��4L=4��48L����2���Ʊ�MnSO4���ٸ�����Ϣ��pHС��7��1������������ȫ��ɳ���ʱ��pH��Ksp[Al(OH)3]=1��10��33=c(Al3��)��c3(OH��)��c(Al3��)=1��10��6mol��L��1���ó���c(OH��)=1��10��9mol��L��1��c(H��)=Kw/c(OH��)=10��5��pH=5��ͬ�������Fe(OH)3��ȫ��ɳ���ʱ��pHԼΪ3��5���ʷ�Χ�ǣ�5��0<pH<7��1����3����MnSO4��MgSO4�����Һ�нᾧMnSO4��H2O���壬����ͼ����Ϣ������60���Ժ�MnSO4��H2O���ܽ�ȼ�С����MgSO4��6H2O���ܽ��������˿��ƽᾧ�¶ȷ�Χ�Ǹ���60�棬�������Եõ�������MnSO4��H2O����4������������ԭ��Ӧ�е�ʧ�����غ㣺n(Mn3��)��1=n(Fe2��)��1=20��00��10��3��0��0500mol=1��00��10��3mol������MnԪ���غ㣬m��MnSO4��H2O��=1��00��10��3��169g=0��169g�������ǣ�0��169/0��1710��100%=98��8%��


 ͬ����ϰǿ����չϵ�д�
ͬ����ϰǿ����չϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ�ֳ��õ�ζ�������ݹ���Ҫ������NaCl�ĺ�����Ӧ����15 g /100 mL��Ī�����ǽϼ�һ�ֲ���Cl-�����ķ������ֲ��ø÷�����ij���۽����Ƿ����NaCl������Ҫ��ʵ��ԭ������(25��)��Ag++ Cl-=" AgCl" ����ɫ��Ksp(AgCl)=1.8��l0-10
2 Ag++ Cr042-= Ag2Cr04��ש��ɫ��Ksp(Ag2Cr04)=1.2��10-12
ȷ��ȡ������Ʒ5.00 mLϡ����100 mL��������ȡ��10.00 mL������ƿ�У��������м��������ĸ������Һ����0.1000 mol/L������������Һ�ζ����ظ�ʵ�����Ρ�
��1����Ʒϡ�����У��� ��ȡ������Ʒ��Ӧ�� �ж��ݣ������õ��IJ���
������_____________��
��2������������Һ����ɫ�ζ���ʢװ��ԭ����__________���ζ����۾�Ӧע�� ������ ���ﵽ�ζ��յ㡣

��3���ζ�����ʱ���ζ�����Һ������ͼ��ʾ�������Ϊ_____________��
��4����������������������Һ��ƽ�����Ϊ12.50 mL����ϡ�ͺ�Ľ�����NaCl��Ũ��Ϊ mol/L�������۽����Ƿ����NaCl������ ����������������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X(g)+2Y(s) ![]() 2Z(g) ��H=-akJ/mol��һ�������£���1molX��2molY����2L�ĺ����ܱ������У�10min����Y�����ʵ���Ϊ1.4mol������˵����ȷ����
2Z(g) ��H=-akJ/mol��һ�������£���1molX��2molY����2L�ĺ����ܱ������У�10min����Y�����ʵ���Ϊ1.4mol������˵����ȷ����
A. 10min�ڣ�X��ƽ����Ӧ����Ϊ0.03mol/(L��min)
B. �������е������ܶȲ��ٷ����仯��˵��������Ӧ�Ѵ�ƽ��״̬
C. 10min��Z��Ũ��Ϊ0.7mol/L
D. 10min�ڣ���Ӧ�ų�������Ϊ0.3kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��þ���仯����һ����(��Ͷ�)������Ⱦ����þԭ��طŵ�ʱ��ѹ�߶�ƽ�⣬ʹþԭ���Խ��Խ��Ϊ����������ɫԭ��صĹ�ע���㡣����һ��þԭ��صķ�ӦΪxMg��Mo3S4![]() MgxMo3S4����þԭ��طŵ�ʱ������˵��������� ( )
MgxMo3S4����þԭ��طŵ�ʱ������˵��������� ( )
A��Mg2��������Ǩ��
B��������ӦΪ��Mo3S4��2xe��===Mo3S![]()
C��Mo3S4����������Ӧ
D��������ӦΪ��xMg��2xe��===xMg2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʮ���ƣ�12CaO��7Al2O3)�����͵ij������Ϻͷ�����ϣ��ð���ʯ����Ҫ��CaCO3��MgCO3)�ͷ�AlƬ�Ʊ�����ʮ���ƵĹ������£�
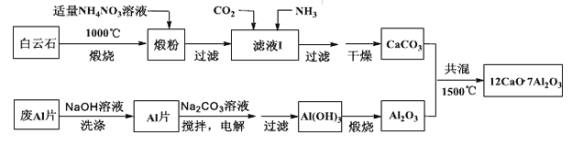
��1���ѷ���Ҫ��MgO�� ����������NH4NO3��Һ��ȡ�ѷۺ�þ�����X�����ܣ� ����ҺI��c(Mg2+)С��5��10-6mol��L-1,����ҺpH���� ��Mg(OH)2��Ksp=5��10-12)���ù����в����ã�NH4)2SO4����NH4NO3��ԭ���� ��
��2����ҺI�е��������� ���������ʳɷֵ�Ӱ�죩������ҺI�н�ͨ��CO2�������� ���Ӷ�����CaCO3���ʽ��͡�
��3����NaOH��Һ�ɳ�ȥ��AlƬ���������Ĥ����Ӧ�����ӷ���ʽΪ ��
��4������Ʊ�Al(OH)3ʱ���缫�ֱ�ΪAlƬ��ʯī������ܷ�Ӧ����ʽΪ ��
��5��һ�ֿɳ��������������أ���ŵ�ʱAlCl4����Al2Cl7������������Al�缫���ת�����������Ӳ�����缫��Ӧ���ŵ�ʱ����Al�ĵ缫��ӦʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����AlƬ��CuƬ�õ������ӣ�һ�����Ũ�����У�һ�����ϡ����������Һ�У��ֱ��γɵ�ԭ��أ���������ԭ����У������ֱ�Ϊ�� ��
A.CuƬ��AlƬ
B.AlƬ��CuƬ
C.AlƬ��AlƬ
D.CuƬ��CuƬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������(Na2S2O5)�dz��õ�ʳƷ��������֮һ��ij�о�С���������ʵ�飺
ʵ��һ ���������Ƶ���ȡ
������ͼװ�ã�ʵ��ǰ�ѳ���װ���ڵĿ�������ȡNa2S2O5��װ�â�����Na2S2O5���������������ķ�ӦΪNa2SO3+SO2= Na2S2O5��

��1��װ�â��в�������Ļ�ѧ����ʽΪ______________________________��
��2��Ҫ��װ�â��л���������ľ��壬�ɲ�ȡ�ķ��뷽����________��
��3��װ�â����ڴ���β������ѡ�õ������װ��(�г���������ȥ)Ϊ________(�����)��

ʵ��� ���������Ƶ�����
��֪��Na2S2O5����ˮ������NaHSO3��
��4�����Na2S2O5�����ڿ������ѱ�������ʵ�鷽���� ____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�һ��̬����������������ȫȼ�գ��ָ������£�ʹȼ�ղ���ͨ��Ũ���ᣬ����ȷ�Ӧǰ����50mL����ͨ��NaOH��Һ������ּ�����40mL��ԭ���ķ���ʽ��( )
A��CH4 B��C4H10 C��C2H6 D��C3H8
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ��0.1 mol/L Na2CO3��Һ�еμӷ�̪����Һ��� B. Al3����NO3����Cl����CO32����Na���ɴ���������pH=2����Һ�� C. �Ҵ������ᶼ������ˮ�����ǵ���� D. �ֱ�������ʵ�����HCl��H2SO4��Ӧʱ������NaOH�����ʵ�����ͬ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com