
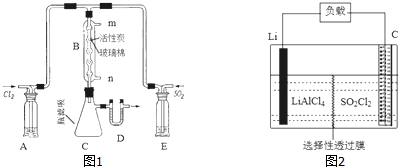
分析 (1)提高反应中Cl2的平衡转化率,即改变条件使平衡向正反应移动,根据平衡移动原理结合选项分析解答,注意不能只增大氯气的用量;
(2)300℃时,在体积为1L的密闭容器中充入16.20g SO2Cl2,发生反应:SO2Cl2(l)?SO2(g)+Cl2(g)△H=+97.3kJ/mol.然后根据n=$\frac{m}{M}$计算SO2的物质的量,由方程式Cl2的物质的量等于SO2的物质的量,计算二者的浓度,则300℃时分解SO2Cl2反应的平衡常数带入K=$\frac{c(S{O}_{2})c(C{l}_{2})}{c(S{O}_{2}C{l}_{2})}$计算可得,而300℃时合成SO2Cl2反应的平衡常数与之互为倒数;
(3)①a.根据饱和食盐水和饱和NaHSO3溶液起不到干燥的作用判断;
b.B处反应管内五球中玻璃棉上的活性炭对氯气和二氧化硫的反应起催化作用;
c.根据B处反应管冷却水应低处进高处出判断;
d.根据反应放热,则装置C处吸滤瓶应放在冰水中冷却有利于利平衡正向移动判断;
e.根据D处U形管中盛放的固体干燥剂判断;
②SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,正反应是放热反应,所以水冷却利于SO2Cl2的合成;
③氯磺酸(C1SO3H)加热分解,也能制得硫酰氯(SO2Cl2)与另外一种物质,由元素守恒可知,另外物质含有H元素,C1SO3H中S、Cl原子数目之比为1:1,而SO2Cl2中S、Cl原子数目之比为1:2,故另外物质中含有S元素,结合原子守恒可知另外物质为H2SO4;二者为互溶液体,沸点相差较大,采取蒸馏法进行分离;
(4)正极是SO2Cl2中+6价的硫得电子发生还原反应,据此书写.
解答 解:(1)提高反应中Cl2的平衡转化率,改变条件使平衡向正反应移动,不能只增大氯气的用量,
a.缩小容器体积,压强增大,平衡向正反应移动,Cl2的转化率增大,故a正确;
b.使用催化剂,缩短到达平衡的时间,不影响平衡移动,Cl2的转化率不变,故b错误;
c.增加SO2浓度,平衡向正反应移动,Cl2的转化率增大,故c正确;
d.该反应正反应是放热反应,提高温度,平衡向逆反应移动,Cl2的转化率降低,故d错误;
故答案为:ac;
(2)300℃时,在体积为1L的密闭容器中充入16.20gSO2Cl2,发生反应:SO2Cl2(g)?SO2(g)+Cl2(g),SO2的物质的量为$\frac{7.616g}{64g/mol}$=0.119mol,由方程式可知,n(Cl2)=n(SO2)=0.119mol,二者浓度都为$\frac{0.119mol}{1L}$=0.119mol/L,故参加反应的SO2Cl2的物质的量为0.119mol,SO2Cl2的物质的量为$\frac{16.2g}{135g/mol}$=0.12mol,平衡时SO2Cl2的物质的量为0.12mol-0.119mol=0.001mol,故SO2Cl2的平衡浓度为$\frac{0.001mol}{1L}$=0.001mol/L,300℃时分解SO2Cl2反应的平衡常数K=$\frac{c(S{O}_{2})c(C{l}_{2})}{c(S{O}_{2}C{l}_{2})}$=$\frac{1.119×0.119}{0.001}$,所以300℃时合成SO2Cl2反应的平衡常数K=$\frac{0.001}{1.119×0.119}$=0.0706;
故答案为:0.0706;
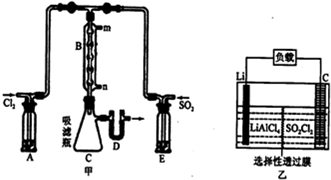
(3)①a.A、E处洗气瓶,干燥吸水,二氧化硫和氯气都可以用浓硫酸干燥,而饱和食盐水和饱和NaHSO3溶液起不到干燥的作用,故a错误;
b.B处反应管内五球中玻璃棉上的活性炭对氯气和二氧化硫的反应起催化作用,故b正确;
c.B处反应管冷却水应低处进高处出,所以从n接口通入,故c错误;
d.装置C处吸滤瓶应放在冰水中冷却,利平衡正向移动,提高产率,故d正确;
e.D处U形管中盛放的固体干燥剂,可能是固体碱石灰,故e正确;
故选:bde;
②SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,正反应是放热反应,所以水冷却利于SO2Cl2的合成,故答案为:冷凝、降温均有利于SO2Cl2生成;
③氯磺酸(C1SO3H)加热分解,也能制得硫酰氯(SO2Cl2)与另外一种物质,由元素守恒可知,另外物质含有H元素,C1SO3H中S、Cl原子数目之比为1:1,而SO2Cl2中S、Cl原子数目之比为1:2,故另外物质中含有S元素,结合原子守恒可知另外物质为H2SO4,反应方程式为:2C1SO3H$\frac{\underline{\;\;△\;\;}}{\;}$SO2Cl2+H2SO4,二者为互溶液体,沸点相差较大,采取蒸馏法进行分离;
故答案为:2C1SO3H$\frac{\underline{\;\;△\;\;}}{\;}$SO2Cl2+H2SO4;蒸馏;
(4)正极是SO2Cl2中+6价的硫得电子发生还原反应,所以电极反应式为:SO2Cl2+2e-=2Cl-+SO2↑,故答案为:SO2Cl2+2e-=2Cl-+SO2↑.
点评 本题考查实验制备方案,涉及对反应原理及操作的分析评价、物质的分离提纯、化学平衡常数的计算以及平衡移动原理等,注意对物质性质信息的应用,难度中等.


 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 有机物A属于醛类 | B. | 有机物A与B属于同系物 | ||
| C. | 有机物C能与H2发生加成反应 | D. | 有机物D的一氯代物有2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
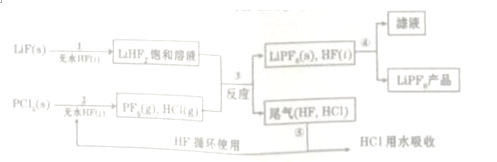
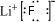 ,无水HF的作用是反应物和溶剂
,无水HF的作用是反应物和溶剂查看答案和解析>>
科目:高中化学 来源: 题型:解答题

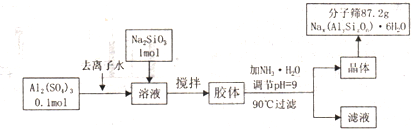
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 都能与氢氧化钠发生中和反应 | B. | 都能使紫色石蕊试液变红 | ||
| C. | 都能发生酯化反应 | D. | 都能和金属钠反应生成H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com