
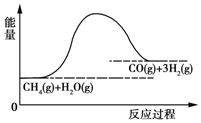
 合成氨用的H2可以CH4为原料制得:CH4(g)+H2O(g)═CO(g)+3H2(g).反应过程的能量变化如图所示,关于该反应的下列说法中,正确的是( )
合成氨用的H2可以CH4为原料制得:CH4(g)+H2O(g)═CO(g)+3H2(g).反应过程的能量变化如图所示,关于该反应的下列说法中,正确的是( )| A. | △H<0,△S<0 | B. | △H>0,△S<0 | C. | △H<0,△S>0 | D. | △H>0,△S>0 |
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用蒸馏水洗净酸式滴定管后,装入标准盐酸进行滴定 | |
| B. | 用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗,后装入NaOH溶液进行滴定 | |
| C. | 用碱式滴定管取10.00mLNaOH溶液放入用蒸馏水洗净的锥形瓶中进行滴定 | |
| D. | 用酚酞作指示剂滴至红色刚变无色时即停止加盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对盛在烧杯(敞口)内的氨水加热,氨水中NH4+浓度减小 | |
| B. | 对2HI(g)?H2(g)+I2(g),保持容器体积不变,通入氢气可使平衡体系颜色变浅 | |
| C. | 500℃左右比室温更有利于合成氨的反应 | |
| D. | 高压有利于合成氨的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
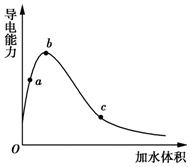 一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下列说法正确的是( )
一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下列说法正确的是( )| A. | a、b、c三点溶液的pH:c<a<b | |
| B. | 用湿润的pH试纸测量a处溶液的pH,测量结果偏小 | |
| C. | a、b、c三点CH3COOH的电离程度:c<a<b | |
| D. | a、b、c三点溶液用1 mol•L-1 NaOH溶液中和,消耗NaOH溶液体积:c<a<b |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
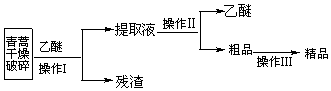
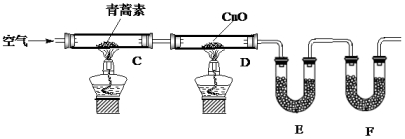
| 装置 | 实验前 | 实验后 |
| E | 24.00g | 33.90g |
| F | 100.00g | 133.00g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性溶液中:Na+、Cl-、OH-、CO32- | B. | 碱性溶液中:Fe3+、NH4+、HCO3-、Cl- | ||
| C. | 无色溶液中:Na+、Cu2+、MnO4-、I- | D. | 透明溶液中:Na+、Fe3+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3 溶液中:c(H+)+c(H2CO3)═c(CO32-)+c(OH-) | |
| B. | 0.1 mol/L醋酸钠溶液20 mL与0.1 mol/L盐酸10 mL混合后的溶液中:c(CH3COO-)>c(Cl-)>c(H+)>c(CH3COOH) | |
| C. | 物质的量浓度相等的①NH4Cl、②(NH4)2SO4、③NH4Al(SO4)2三种溶液中,c(NH4+) 由大到小的顺序为③>②>① | |
| D. | 浓度均为0.1 mol/L的①氨水、②NaOH溶液、③Na2CO3溶液、④NaHCO3溶液,pH的大小顺序;②>③>④>① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com