
| A���÷�Ӧ��ƽ��ʱH2��ת����Ϊ40% |
| B�������¶���ʹ���������ܶ����� |
| C����������г���N2��ƽ�������ƶ� |
| D���з���Ч�����ɴ�����N2��ת���� |
| 1.2mol |
| 4mol |
| m |
| V |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ���ٵƾ���ʹ�������������ܻ������ŵ㣮һ���¶��£��ڵ��ٵƵ����ڷ���������������ڵ��ݱ��ϵ��ٿ��Է������µĿ��淴Ӧ��
���ٵƾ���ʹ�������������ܻ������ŵ㣮һ���¶��£��ڵ��ٵƵ����ڷ���������������ڵ��ݱ��ϵ��ٿ��Է������µĿ��淴Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��10�֣����ٵƾ���ʹ�������������ܻ������ŵ㡣һ���¶��£��ڵ��ٵƵ����ڷ���������������ڵ��ݱ��ϵ��ٿ��Է������µĿ��淴Ӧ��
W��s��+ I2��g�� WI2��g����H<0
Ϊģ��������Ӧ����450��ʱ��һ���Ϊ2L�ĺ����ܱ������м���0.1mol�ⵥ�ʺ��������٣�2min��Ӧ�ﵽƽ�⣬��õ�����Ũ��Ϊ0.005 mol��L-1����ش��������⣺
��1��ǰ�������ڵ������ķ�Ӧ����Ϊ �� ��
��2���ܹ�˵��������Ӧ�Ѿ��ﵽƽ��״̬���� �� ��
A��I2��WI2��Ũ�����
B������������ѹǿ���ٱ仯
C��W���������ٱ仯
D����λʱ���ڣ����������ĵ����ʵ�����⻯�����ɵ����ʵ������
E�������ڻ��������ܶȱ��ֲ���
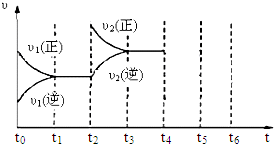
��3����ͼΪ�÷�Ӧ��450��ʱ��ʱ�䡪����ͼ����t2ʱ�̸ı��������������� �� ����t4ʱ�̽�����ѹ����һ�루������״̬���䣩�����ָ�������t6������ͼ�л���t4��t6ʱ����ڴ�������ͼ��������Ӧ�����ϱ��Ϧ�3(��)����3(��)
t0 t1 t2 t3 t4 t5 t6 t
��4�������˿�¶�Ϊ660�棬���ݱ��¶�Ϊ350�档����ݻ�ѧ��Ӧԭ�������ڵ����ڳ�����ܹ��ӳ���˿������ԭ�� �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013��ȱ�Ϫ�и�һ��ѧ����ĩ���Ի�ѧ�Ծ� ���ͣ�ѡ����
��һ���Ϊ2L�ĺ����ܱ����������1
mol N2��4 molH2����һ���¶��·�����Ӧ�� N2��g��+3H2��g��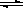 2NH3��g������H<0��10���ﵽƽ�⣬c��NH3��Ϊ0.4mol/L������˵����ȷ����
2NH3��g������H<0��10���ﵽƽ�⣬c��NH3��Ϊ0.4mol/L������˵����ȷ����
A���÷�Ӧ��ƽ��ʱH2��ת����Ϊ40%
B�������¶���ʹ���������ܶ�����
C����������г���N2��ƽ�������ƶ�
D���з���Ч�����ɴ�����N2��ת����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com