
 �����仯�����������������ϵ���У�
�����仯�����������������ϵ���У�| c(CO2) |
| c(CO) |
| c(CO2) |
| c(CO) |
| 0.01 |
| x-0.01 |


 ����ȫ���ִʾ��ƪ��ϵ�д�
����ȫ���ִʾ��ƪ��ϵ�д� �����߿����ϵ�д�
�����߿����ϵ�д� �㾦�½̲�ȫ�ܽ��ϵ�д�
�㾦�½̲�ȫ�ܽ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢ڢۢܢݢޢ� |
| B���٢ۢܢݢޢ� |
| C���٢ۢܢޢ� |
| D���٢ۢݢޢߢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��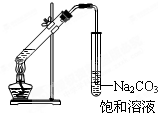 ʵ���ҳ�����ͼ��ʾ��װ����ȡ�������������� |
| B�����ȵĴ�����Һϴ���Թ��ڱڸ��ŵ���֬ |
| C�����ھƾ��ƵĻ��������պ������ս���ëζ |
| D���ñ���ȡ��ˮ�е��壬��Һʱ�л���ӷ�Һ©�����¶˷ų� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 Ԫ��Xλ�ڵ������ڣ����̬ԭ�ӵ��ڲ���ȫ���������ӣ�������������Ϊ2��Ԫ��Y��̬ԭ�ӵ�3p�������4�����ӣ�Ԫ��Z��ԭ�����������������ڲ��3����
Ԫ��Xλ�ڵ������ڣ����̬ԭ�ӵ��ڲ���ȫ���������ӣ�������������Ϊ2��Ԫ��Y��̬ԭ�ӵ�3p�������4�����ӣ�Ԫ��Z��ԭ�����������������ڲ��3�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
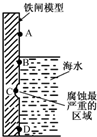
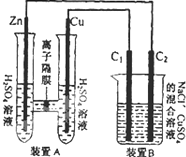 ����ͼװ�ã��ش��������⣺
����ͼװ�ã��ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��200mlij���������1.5NA��SO
| ||
| B��һ��������������Fe����Ũ���ᷴӦ��ת�Ƶ�����һ��Ϊ2NA | ||
| C�����³�ѹ��78gNa2O2������������������������Ϊ4NA | ||
| D����⾫��ͭʱ���������õ�������Ϊ2NA����������64g |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com