
| A�� | ��м����ϡ���2Fe+6H+�T2Fe3++3H2�� | |
| B�� | AlCl3��Һ�м������ϡ��ˮ��Al3++4NH3•H2O�TAlO2-+4NH4++2H2O | |
| C�� | AlƬ����NaOH��Һ�У��������壺2Al+2OH-+2H2O�T2AlO2-+3H2�� | |
| D�� | NaOH��Һ�еμ�����Al2��SO4��3��Һ��Al3++3OH-�TAl��OH��3�� |
���� A������ϡ���ᷴӦ���ɵ����������ӣ�
B�����߷�Ӧ������������������
C����������������Һ��Ӧ����ƫ�����ƺ�������
D����������������Ӧ����ƫ�����ƣ�����������������������
��� �⣺A����м����ϡ���������Ȼ���������������ȷ�����ӷ���ʽΪ��Fe+2H+�TFe2++H2������A����
B��һˮ�ϰ�Ϊ���������������������������ȷ�����ӷ���ʽΪ��Al3++3NH3•H2O=Al��OH��3��+3NH4+����B����
C��AlƬ����NaOH��Һ�У�����ƫ�����ƺ���������Ӧ�����ӷ���ʽΪ��2Al+2OH-+2H2O�T2AlO2-+3H2������C��ȷ��
D��NaOH��Һ�еμ�����Al2��SO4��3��Һ����Ӧ����ƫ�����ƺ������ƣ���ȷ�����ӷ���ʽΪ��Al3++4OH-�TAlO2-+2H2O����D����
��ѡC��
���� ���⿼�������ӷ���ʽ����д�жϣ�Ϊ�߿��ĸ�Ƶ�⣬�����е��Ѷȵ����⣬ע���������ӷ���ʽ����дԭ����ȷ���ӷ���ʽ�����жϳ��÷�������鷴Ӧ��������Ƿ���ȷ���������ʲ���Ƿ���ȷ���������������ʵ���Ҫ������ѧʽ������Ƿ����ԭ��ѧ����ʽ�ȣ�������ؿ��������ʼ��仯�������ʵĿ��飮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
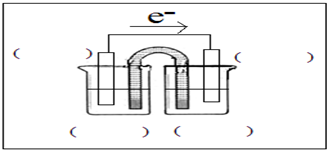 ����֮������ת����ԭ��ؿɽ���ѧ��ת��Ϊ���ܣ�
����֮������ת����ԭ��ؿɽ���ѧ��ת��Ϊ���ܣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2O2����ˮ����O2��Na2O2+H2O�T2Na++2OH-+O2�� | |
| B�� | Fe��OH��3��������Fe��OH��3+3H+�TFe3++3H2O | |
| C�� | ���������Һ��ͨ�����������̼��Ca2++2ClO-+H2O+CO2�TCaCO3��+2HClO | |
| D�� | ��һ������AlƬͶ��������NaOH��Һ�У�2Al+2OH-+2H2O�T2AlO2-+3H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������ڱ�״����Ϊ2.24L | |
| B�� | ��Ӧ����Һ��c ��Fe3+��=0.125mo1/L | |
| C�� | ��Ӧ�����Һ��Ͷ��2.8g���ۿ�ȫ���ܽ� | |
| D�� | ��Ӧ����Һ��c��NO3-��=0.75mo1/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ClO4-��Cl-��Na+ | B�� | ClO-��Cl-��H+ | C�� | NaClO��NaClO3 | D�� | NaClO��NaCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ѿ�� | B�� | ���� | C�� | ��ά�� | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ۢܢ� | B�� | �٢ۢܢ� | C�� | �ڢۢޢ� | D�� | �ۢܢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ�ѧ����ʽ�л�ѧ��������ʾ���Ӹ��� | |
| B�� | Q=483.6 | |
| C�� | Q��483.6 | |
| D�� | Q��483.6 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com