
����Ŀ����ʽ̼����[Cox(OH)y(CO3)z]���������Ӳ��ϣ����Բ��ϵ����Ӽ�������ʱ�ɷֽ��������������Ϊ��ȷ������ɣ�ij��ѧ��ȤС��ͬѧ�������ͼ��ʾװ�ý���ʵ�顣

(1)���������ʵ�鲽�裺
�ٳ�ȡ3.65 g��Ʒ����Ӳ�ʲ������ڣ������ҡ���װ�õ�������
�ڰ���ͼ��ʾװ����װ��������������װ�������ԣ�
�ۼ��ȼ��в����ܣ�����װ����________________(������)��ֹͣ���ȣ�
�ܴ���a������ͨ����������Ӻ����ҡ���װ�õ�������
�ݼ��㡣
(2)������л���ͨ����������ӵ�Ŀ����___________________________��
(3)ijͬѧ��Ϊ����ʵ��װ���д���һ������ȱ�ݣ�Ϊ�����һ���⣬��ѡ������װ���е�____________(����ĸ)������________(��װ������λ��)��

(4)������ȷװ�ý���ʵ�飬����������ݣ���ü�ʽ̼���ܵĻ�ѧʽΪ______��
��װ�õ�����/g | ��װ�õ�����/g | |
����ǰ | 80.00 | 62.00 |
���Ⱥ� | 80.36 | 62.88 |
(5)CoCl2��6H2O���������ˮ������Ӽ����Ժ��ܷ���(������Fe��Al������)��ȡCoCl2��6H2O��һ�ֹ������£�

��֪��
������ | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
��ʼ����(pH) | 2.3 | 7.5 | 7.6 | 3.4 |
��ȫ����(pH) | 4.1 | 9.7 | 9.2 | 5.2 |
�پ���������ʱ������H2O2������Ӧ�����ӷ���ʽΪ___________________��
�ڼ���CoCO3��pHΪ5.2��7.6����������õ������ɷ�Ϊ_____________��
�ۼ��������pHΪ2��3��Ŀ��Ϊ________________________________��
���𰸡����������ݲ���ʱ ��װ���в�����CO2��H2O(g)ȫ�������ҡ���װ���� D ����aǰ(��װ�ü�ǰ) Co3(OH)4(CO3)2 2Fe2����H2O2��2H����2Fe3����2H2O Al(OH)3��Fe(OH)3 ����CoCl2��ˮ��
��������
��1�����ȼ��в����ܣ�����װ���в��������ݲ���������ʽ̼���ֽܷ���ϣ�
��2��������л���ͨ����������ӣ���װ�������ɵ�CO2��H2Oȫ�������ҡ���װ���У�����Ӱ����������
��3���ڻ���aǰ����װװ��D��װ����ʢ�ŵļ�ʯ���������տ����е�ˮ�����Ͷ�����̼��
��4����ʽ̼������Ʒ3.65g����Ӧǰ��װ�õ�����Ϊ80.00g����Ӧ������Ϊ80.36g��������ˮ������Ϊ80.36g-80.00g=0.36g�����ʵ���Ϊ![]() =0.02mol����Ӧǰ��װ�õ�����Ϊ62.00g����Ӧ������Ϊ62.00g�����ɶ�����̼������Ϊ62.88g-62.00g=0.88g�����ʵ���Ϊ
=0.02mol����Ӧǰ��װ�õ�����Ϊ62.00g����Ӧ������Ϊ62.00g�����ɶ�����̼������Ϊ62.88g-62.00g=0.88g�����ʵ���Ϊ![]() =0.02mol����Co������Ϊ3.65g-0.02mol��2��17g/mol-0.02mol��60g/mol=1.77g����Coԭ�����ʵ���Ϊ��
=0.02mol����Co������Ϊ3.65g-0.02mol��2��17g/mol-0.02mol��60g/mol=1.77g����Coԭ�����ʵ���Ϊ��![]() =0.03mol���ٽ���غ㷨�����ʽ̼���ܵĻ�ѧʽ��
=0.03mol���ٽ���غ㷨�����ʽ̼���ܵĻ�ѧʽ��
��5�����ܷ����м������ϡ���ᣬFe��Al��ϡ���ᷴӦ����FeCl2��AlCl3��CoCl2������Һ�м���˫��ˮ��CoCO3��˫��ˮ����ǿ�����ԣ��ܽ�������������Ϊ�����ӣ����ӷ�Ӧ����ʽΪ2Fe2++H2O2+2H+=2Fe3++2H2O������CoCO3��������Һ��pH��7.6��ʹFe��OH��3��Al��OH��3���ɳ�����Ȼ����ˣ�����ΪFe��OH��3��Al��OH��3����Һ�к���CoCl2��Ȼ������Һ�м���ϡ���ᣬ����CoCl2ˮ�⣬Ȼ���������Ũ������ȴ�ᾧ���˷����õ�CoCl26H2O��
��˫��ˮ���������ԣ���������ԭ�����ӣ�
�ڼ���CoCO3��pHΪ5.2��7.6�������I��õ������ɷ�ΪFe��OH��3��Al��OH��3��
��CoCl2Ϊǿ�������Σ�������ˮ�����Һ�����ԣ�����ϡ����������ˮ�⡣
��1�����ȼ��в����ܣ�����װ���в��������ݲ���������ʽ̼���ֽܷ���ϣ�
��2��������л���ͨ����������ӣ���װ�������ɵ�CO2��H2Oȫ�������ҡ���װ���У�����Ӱ����������
��3���ڻ���aǰ����װװ��D��װ����ʢ�ŵļ�ʯ���������տ����е�ˮ�����Ͷ�����̼��
��4����ʽ̼������Ʒ3.65g����Ӧǰ��װ�õ�����Ϊ80.00g����Ӧ������Ϊ80.36g��������ˮ������Ϊ80.36g-80.00g=0.36g�����ʵ���Ϊ![]() =0.02mol����Ӧǰ��װ�õ�����Ϊ62.00g����Ӧ������Ϊ62.00g�����ɶ�����̼������Ϊ62.88g-62.00g=0.88g�����ʵ���Ϊ
=0.02mol����Ӧǰ��װ�õ�����Ϊ62.00g����Ӧ������Ϊ62.00g�����ɶ�����̼������Ϊ62.88g-62.00g=0.88g�����ʵ���Ϊ![]() =0.02mol����Co������Ϊ3.65g-0.02mol��2��17g/mol-0.02mol��60g/mol=1.77g����Coԭ�����ʵ���Ϊ��
=0.02mol����Co������Ϊ3.65g-0.02mol��2��17g/mol-0.02mol��60g/mol=1.77g����Coԭ�����ʵ���Ϊ��![]() =0.03mol������Co��H��CԪ���غ��֪��x��y��z=0.03mol��0.02mol��2��0.02mol=3��4��2���ʼ�ʽ̼���ܵĻ�ѧʽΪCo3��OH��8��CO3��4��
=0.03mol������Co��H��CԪ���غ��֪��x��y��z=0.03mol��0.02mol��2��0.02mol=3��4��2���ʼ�ʽ̼���ܵĻ�ѧʽΪCo3��OH��8��CO3��4��
��5�����ܷ����м������ϡ���ᣬFe��Al��ϡ���ᷴӦ����FeCl2��AlCl3��CoCl2������Һ�м���˫��ˮ��CoCO3��˫��ˮ����ǿ�����ԣ��ܽ�������������Ϊ�����ӣ����ӷ�Ӧ����ʽΪ2Fe2++H2O2+2H+=2Fe3++2H2O������CoCO3��������Һ��pH��7.6��ʹFe��OH��3��Al��OH��3���ɳ�����Ȼ����ˣ�����ΪFe��OH��3��Al��OH��3����Һ�к���CoCl2��Ȼ������Һ�м���ϡ���ᣬ����CoCl2ˮ�⣬Ȼ���������Ũ������ȴ�ᾧ���˷����õ�span>CoCl26H2O��
��˫��ˮ����ǿ�����ԣ��ܽ�������������Ϊ�����ӣ����ӷ�Ӧ����ʽΪ2Fe2++H2O2+2H+=2Fe3++2H2O��
�ڼ���CoCO3��pHΪ5.2��7.6�������I��õ������ɷ�ΪFe��OH��3��Al��OH��3��
��CoCl2Ϊǿ�������Σ�������ˮ�����Һ�����ԣ�����ϡ����������ˮ�⣬���Լ���ϡ�����Ŀ��������CoCl2ˮ�⡣


 ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д�
ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͬ�������ķ�ͭƬ���ֱ������������������У���һ�������·�Ӧ�����õ�����������ʵ���������(����)
A.Ũ����B.ϡ����C.Ũ����D.ϡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڸ��������£�����ѡ����ʾ�����ʼ�ת������ʵ�ֵ��ǣ� ��
A.Fe(s)![]() FeCl3(s)
FeCl3(s)![]() Fe(OH)3(s)
Fe(OH)3(s)
B.CaCl2(aq)![]() CaCO3(s)
CaCO3(s)![]() CaO(s)
CaO(s)
C.NaHCO3(s)![]() Na2CO3(s)
Na2CO3(s)![]() NaOH(s)
NaOH(s)
D.Al2O3(s)![]() AlCl3(aq)
AlCl3(aq) ![]() Al(OH)3 (s)
Al(OH)3 (s)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾװ�ôӺ�ˮ����ȡCO2,�����ڼ��ٻ�������������ĺ���������˵����ȷ����

A. ͨ���a�ҵ�pH����
B. �м���ҷ����ķ�Ӧ:HCO3-+H+==CO2��+H2O���Ӷ���ȡCO2
C. ������ӦʽΪ2H+-2e-==H2��
D. ����·��ͨ��1mol���ӵĵ���ʱ������22.4LCO2�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������(M)��ҽҩ�����ϵ��м��壬ʵ�����ɷ��㻯����A�Ʊ�M��һ�ֺϳ�·�����£�

��֪���� (R1��R2��ʾ��ԭ�ӻ�����)
(R1��R2��ʾ��ԭ�ӻ�����)
��R1COOR2��R3CH2COOR4![]()
 ��R2OH
��R2OH
(R1��R3��ʾ��ԭ�ӻ�������R2��R4��ʾ����)
��ش��������⣺(1)A��B������Ϊ________��
(2)E�����������ŵ�����Ϊ________��
(3)H�Ľṹ��ʽΪ________��(4)I��M�ķ�Ӧ����Ϊ________��
(5)D��F��G�Ļ�ѧ����ʽΪ________________________��
(6)ͬʱ��������������I��ͬ���칹����________��(�����������칹)����дһ�ֺ˴Ź�����������6�����շ��ҷ����֮��Ϊ1��2��2��2��2��1�Ľṹ��ʽΪ_______��
���ܷ�����ɫ��Ӧ��������Ӧ���ڱ�������������ȡ����
(7)�������� ��Ϣ���Լ���ͱ���Ϊԭ��(�������Լ���ѡ)������Ʊ�
��Ϣ���Լ���ͱ���Ϊԭ��(�������Լ���ѡ)������Ʊ� �ĺϳ�·��_______________________��
�ĺϳ�·��_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ����������������γɿ϶��ص��ǣ� ��
A.SO2+2H2S=3S+2H2OB.SO2+H2O![]() H2SO3
H2SO3
C.2SO2+O2![]() 2SO3D.SO3+H2O=H2SO4
2SO3D.SO3+H2O=H2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϩ��ʯ�ͻ�ѧ��ҵ����Ҫ�Ļ���ԭ�ϣ�����ϩΪԭ�Ͽ����Ƶ����ҵ���Ϻ�����Ʒ����ϩ�ܷ�������ת����ϵ��
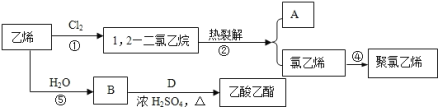
(1)A�ķ���ʽΪ____________��������D�Ĺ�����������_____________��
(2)д����Ӧ�١��ܵĻ�ѧ����ʽ��
��__________��
��__________��
(3)������Ӧ�У��������л�����ΪĿ�꣬ԭ��������100%�ķ�Ӧ��_________________��
(4)ʵ������B��D�Ʊ����������Ļ�ѧ����ʽ��______��Ũ�����������_______ �������ᴿ��Ʒ���õ��Լ���________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���飨As���ǵ�������VA��Ԫ�أ������γ�As2S3��H3AsO3��H3AsO4�Ȼ������;�㷺��
���������գ�
��1����ԭ�Ӻ�����__�����Ӳ㣬�������__�����ӣ�д����ԭ���������ӵĹ����ʾʽ��__��
��2��������VA�����ж�����Ԫ�ص�ԭ�Ӱ뾶������С�����˳�����У�__����Ԫ�ط��ű�ʾ����
��3����λ��VIIA��������ͬ���ڣ��Ƚ��塢������������Ӧˮ�������Ե�ǿ����__ǿ��__�������ʵĻ�ѧʽ����
��4�����ڱ��У������鶼�ڽ����ͷǽ��������߸�������һ��˵����Ԫ�ؾ��зǽ����ԣ�__��
��5����֪��ϡNa3AsO3��Һ��ϡ��ˮ��ϡNaOH��Һ��ϣ��������·�Ӧ��AsO33-(aq)+I2(aq)+2OH-![]() AsO43-(aq)+2I-(aq)+H2O(l)����Һ��c(AsO43-)�뷴Ӧʱ�䣨t���Ĺ�ϵ��ͼ��ʾ��
AsO43-(aq)+2I-(aq)+H2O(l)����Һ��c(AsO43-)�뷴Ӧʱ�䣨t���Ĺ�ϵ��ͼ��ʾ��

��д���÷�Ӧƽ�ⳣ���ı���ʽK=___��
�ڲ����жϷ�Ӧ�ﵽƽ��״̬����___��ѡ���ţ���
A.��Һ��pH���ٱ仯
B.v(I-)=2v(AsO33-)
C.c(AsO33-)/c(I-)���ٱ仯
D.c(I-)=2ymol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�������ܶȻ�������Ksp[Pb��OH��2]=2��10-15��Ksp[Fe��OH��2]=8��10-15������Һ�н�������Ũ��С��10-5molL-1��Ϊ������ȫ����20mL��0.10molL-1Pb2+��0.10molL-1Fe2+�Ļ����Һ�еμ�0.10molL-1NaOH��Һ������������Ũ�������NaOH��Һ����Ĺ�ϵ������ͼ��ʾ��������˵����ȷ���ǣ� ��
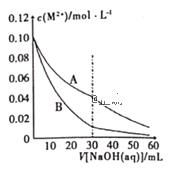
A.����A��ʾc(Pb2+)������
B.����ҺpH=8ʱ��Fe2+��ʼ������Pb2+������ȫ
C.����NaOH��Һ�������30mLʱ����Һ��c(Fe2+)=4c(Pb2+)
D.�����£��μ�NaOH��Һ�����У�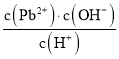 ��ֵ��������
��ֵ��������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com