
| A. | 在0.1 mol NaHSO4晶体中阳离子与阴离子总数为0.2 NA | |
| B. | l L 0.1mol•L-1的H2SO3溶液中含有H+的数目为0.2 NA | |
| C. | 7.8 g Na2O2中含有的阴离子数目为0.1 NA | |
| D. | 常温常压下,14 g乙烯和丙烯的混合气体中氢原子数为 2 NA |
分析 A、硫酸氢钠由1个钠离子和1个硫酸氢根构成;
B、亚硫酸是弱酸,在溶液中不能完全电离;
C、求出过氧化钠的物质的量,然后根据1mol过氧化钠中含2mol钠离子和1mol过氧根构成来分析;
D、乙烯和丙烯的最简式均为CH2.
解答 解:A、硫酸氢钠由1个钠离子和1个硫酸氢根构成,故0.1mol硫酸氢钠中含0.1mol钠离子和0.1mol硫酸氢根离子即共0.2mol即0.2NA个,故A正确;
B、亚硫酸是弱酸,在溶液中不能完全电离,故溶液中的氢离子的个数小于0.2NA个,故B错误;
C、7.8g过氧化钠的物质的量为0.1mol,而1mol过氧化钠中含2mol钠离子和1mol过氧根构成,故0.1mol过氧化钠中含0.1mol阴离子即0.1NA个,故C正确;
D、乙烯和丙烯的最简式均为CH2,故14g混合物中含有的CH2的物质的量为1mol,则含2mol氢原子即2NA个,故D正确.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.


 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:选择题
| 加入溶液 | ①适量铋酸钠溶液 | ②过量的双氧水 | ③适量KI淀粉溶液 |
| 实验现象 | 溶液呈紫红色 | 紫红色消失,产生气泡 | 溶液变成蓝色 |
| A. | I2,H2O2,KMnO4,NaBiO3 | B. | H2O2,I2,NaBiO3,KMnO4 | ||
| C. | NaBiO3,KMnO4,H2O2,I2 | D. | KMnO4,NaBiO3,I2,H2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
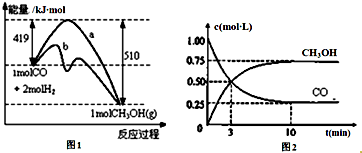 工业上用CO生产燃料甲醇.一定温度和容积条件下发生反应:CO(g)+2H2(g)?CH3OH(g).图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2molH2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化.请回答下列问题:
工业上用CO生产燃料甲醇.一定温度和容积条件下发生反应:CO(g)+2H2(g)?CH3OH(g).图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2molH2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
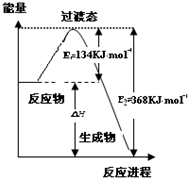 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑥③ | B. | ②③⑥③ | C. | ②③④③ | D. | ②③⑤③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com