
| ���� | ��ʼ����ʱ��pH | ��ȫ����ʱ��pH |
| Fe��OH��3 | 2.2 | 3.2 |
| Fe��OH��2 | 7.6 | 9.6 |
| Cu��OH��2 | 4.7 | 6.4 |
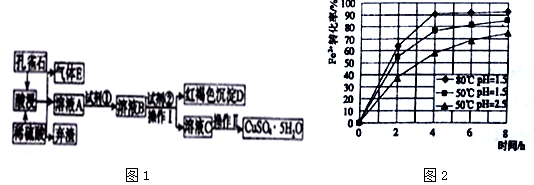
���� ���ȸʯ�м�������ϡ���ᣬ�����ķ�Ӧ��Cu2��OH��2CO3+4HCl=2CuCl2+3H2O+CO2������ҺAֻ��Cu2+��Fe2+��Fe3+���ֽ������ӣ���������������ϡ�����������Ρ������κ�ˮ��Ȼ����˵õ��������к���Si���������ҺA�к��к������κ������μ�����ͭ������EΪCO2������ҺA�м����Լ��ٵõ���ҺB���Լ�����һ������������Fe2+ת��ΪFe3+�Ҳ����������ʣ�Ӧ��ѡȡ˫��ˮ������ҺB�м����Լ��ھ���������õ���ҺC�ͺ��ɫ����D���������Ϊ���ˣ�DΪFe��OH��3����ҺCΪ����ͭ��Һ������Ϊ�Լ���ΪCuO���ݴ˴��⣮
��� �⣺��1�����ݷ�����֪����������Ҫ�ɷ���SiO2�������С�ϴ�ӡ��IJ�������Ŀ���dz�ȥ������渽�ŵ����ʣ��ʴ�Ϊ��SiO2����ȥ������渽�ŵ����ʣ�
��2�����Լ�1����Ŀ���ǽ���Һ�е�Fe2+ת��ΪFe3+���Ҳ����������ʣ�����˫��ˮ��˫��ˮ��һ����ɫ�Լ�����Fe2+����ΪFe3+�������������ʣ���Ӧ���ӷ���ʽΪ 2Fe2++2H++H2O2=2Fe3++2H2O��
�ʴ�Ϊ��b�� 2Fe2++2H++H2O2=2Fe3++2H2O��
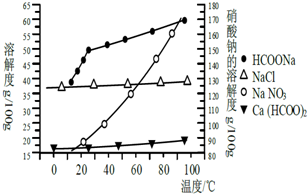
��3��������ͼ2�й����ݿ�֪��pHֵ���ʱ�¶�Խ��Fe2+ת����Խ�ߣ��¶����ʱpHֵԽСFe2+ת����Խ�ߣ����Թ�ҵ����������ʱӦ��ȡ�Ĵ�ʩ����Һ�¶ȿ�����80�棬pH������1.5������ʱ��Ϊ4Сʱ����Fe2+ת���ʴﵽ�ϴ�ֵ��4Сʱ�Ժ�仯����
�ʴ�Ϊ��80�棬pH=1.5��4��
��4������������Ϣ��֪��Cu��OH��2��pH=4.7ʱ��ʼ��������Fe��OH��3��pH=3.2ʱ������ȫ�����Բ���������Һ��pHӦ������3.2��pH��4.7
���ʴ�Ϊ��3.2��pH��4.7��
��5��KMnO4��Һ����ǿ������Ӧ������ʽ�ζ����У�Fe2+��Һ��KMnO4��Һ����������ԭ��Ӧ����Ӧ��MnO4-����ԭΪMn2+����Ӧ�����ӷ���ʽΪMnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O���������ӷ��̿�֪MnO4-��5Fe2+����ȥ KMnO4�����ʵ���Ϊ16.00mL��0.0240mol/L=3.84��10-4mol������A��Һ��Fe2+Ũ��Ϊ$\frac{3.84��10{\;}^{\\;-4}mol��5}{0.02L}$=0.096mol/L��
�ʴ�Ϊ���0.096mol/L��
���� ���⿼�������Ʊ������ʷ�����ᴿ��Ϊ�߿���Ƶ�㣬���ؿ���ѧ�����������㼰ʵ������������ؼ�����ȷʵ��ԭ������������������֪������ͼ�з����ķ�Ӧ�������������ѵ��ǣ�5���ļ��㣬Ҫ������֮���ת������Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����ƹ㷺����ʳƷ��������ʯ�͵ȹ�ҵ�����ϣ�300��400�����ҷֽ⣮
����ƹ㷺����ʳƷ��������ʯ�͵ȹ�ҵ�����ϣ�300��400�����ҷֽ⣮| ���� ���� | ��ʼ���� ��pH | ������ȫ��pH |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ױ����������ױ������� | |
| B�� | ��ȥ����ϩ������������״������� | |
| C�� | ��ȥĮ��������ˮ����Һ | |
| D�� | �Ӵֲ�Ʒ���ᴿ�������ƣ��ؽᾧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2O2�ڷ�Ӧ��ֻ�������� | |
| B�� | ����Na2O2��H2O��Ӧ�ų�������������������֬����ȼ�� | |
| C�� | Na2O2��H2O��Ӧ���������������ɣ�Na2O2�ǵ��͵ļ��������� | |
| D�� | Na2O2��H2O��Ӧ�����������ɣ������ڷ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Al3+��Fe3+��SO42- | B�� | Na+��[Al��OH��4]-��CO32- | ||
| C�� | Na+��[Al��OH��4]-��SO42-��CO32- | D�� | Na+��Ba2+��[Al��OH��4]- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 5.1 g | B�� | 10.2 g | C�� | 13.6 g | D�� | 15.3 g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com