
(13分)已知M是无色液体,C、H、D是有刺激性气味的气体,且D是单质,E为三原子非极性分子,②是工业上制取F的反应,J为漂白粉的有效成份。(部分反应条件未列出)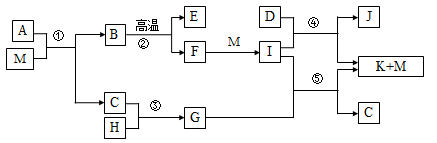
请回答下列问题:
(1)E、D、J的化学式分别是 、 、 ,G的电子式
(2)反应④的化学方程式
(3) 简述C的一种用途:
(4) A由三种元素组成,1 mol A与M反应可生成1 mol B和2 mol C,则A的化学式是
(5)漂白粉常用作消毒剂、杀菌剂、漂白剂等。漂白粉是一种混合物,漂白粉质量高低由"有效氯"(过量酸与漂白粉作用生成的氯气的质量与漂白粉的质量比)决定。漂白粉样品2.00克,加水研磨后,转入250毫升容量瓶内,用水稀释至刻度,摇匀后,取出25.0毫升,加入过量的KI溶液和过量的稀硫酸,静置。待漂白粉放出的氯气与KI完全反应后,用0.100摩/升的Na2S2O3标准溶液滴定反应中生成的碘。反应如下:2Na2S2O3+I2=Na2S4O6+2NaI滴定时用去Na2S2O3溶液20.0毫升。计算该漂白粉中有效氯的百分含量。
已知漂白粉与酸的反应为:Ca(ClO)2+CaCl2+2H2SO4=2CaSO4+2Cl2↑+2H2O
科目:高中化学 来源: 题型:
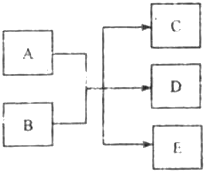 (2011?河西区一模)在一定条件下,物质A~E相互转化的关系如下图所示,其中A为单质,常温下E是无色液体.请根据条件回答下列问题(填写化学用语):
(2011?河西区一模)在一定条件下,物质A~E相互转化的关系如下图所示,其中A为单质,常温下E是无色液体.请根据条件回答下列问题(填写化学用语):

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
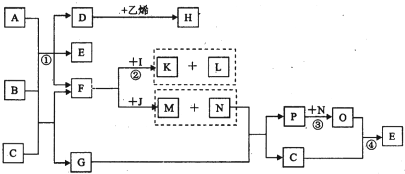
已知甲和I、L、M均为常见的单质,I在常温下为气体,L、M为金属;气体K的水溶液显碱性;A是由前20号元素组成的阴阳离子个数比为1∶1的离子化合物,且阴离子含有14个电子;乙是一种红棕色的粉末,G为白色胶状沉淀,D在常温下是无色液体,C的溶液常用于在实验室检验E。各物质之间的转化关系如下图所示(部分物质在图中没有列出)。

请根据要求填空:
(1)A的化学式为______________________,E的电子式为_______________________。
(2)反应①的化学方程式为___________________________________________________。
(3)反应②的化学方程式为___________________________________________________。
(4)J→G的离子方程式为_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源:0117 期中题 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com