
| A. | 稀氨水 | B. | NaOH溶液 | C. | 硫氰化钾溶液 | D. | Cu2(OH)2CO3固体 |
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
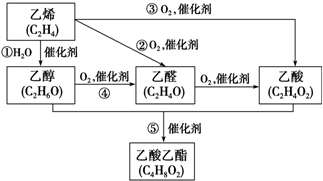 如图是由乙烯合成乙酸乙酯的几种可能的合成路线:
如图是由乙烯合成乙酸乙酯的几种可能的合成路线:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙和盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| B. | 向氢氧化钡溶液中加硫酸溶液:Ba2++SO42-═BaSO4↓ | |
| C. | 向稀盐酸溶液中加铁:3Fe+6H+═3Fe3++3H2↑ | |
| D. | 向硝酸银溶液中加盐酸:Ag++Cl-═AgCl↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸作氧化剂 | B. | HNO3被还原 | ||
| C. | 王水有很强的氧化性 | D. | HAuCl4中Au的化合价为+3价 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
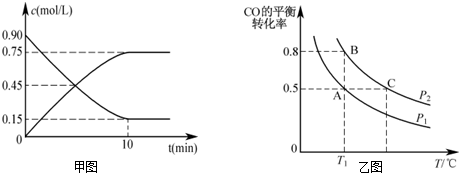
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由石墨制备金刚石是吸热反应;等质量时,石墨的总能量比金刚石低 | |
| B. | 由石墨制备金刚石是吸热反应;等质量时,石墨的总能量比金刚石高 | |
| C. | 由石墨制备金刚石是放热反应;等质量时,石墨的总能量比金刚石低 | |
| D. | 由石墨制备金刚石是放热反应;等质量时,石墨的总能量比金刚石高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.53g | B. | 5.30g | C. | 10.6g | D. | 11.7g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中一定不含Ba2+、Mg2+、SiO32-、Fe2+、SO32- | |
| B. | 该溶液中一定含有AlO2-、Cl-、K+ | |
| C. | 根据①推测可能发生下列反应:HCO3-+AlO2-+H2O═CO32-+Al(OH)3↓ | |
| D. | 原溶液中n(K+)>0.002mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com