
指出下列反应中SiO2所表现的化学性质或作用,在A~E选项中 选择正确答案填入括号内。
选择正确答案填入括号内。
(1)SiO2+2NaOH===Na2SiO3+H2O ( )
(2)SiO2+Na2CO3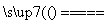 Na2SiO3+CO2↑ ( )
Na2SiO3+CO2↑ ( )
(3)SiO2+2C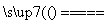 Si+2CO↑ ( )
Si+2CO↑ ( )
(4)SiO2+3C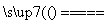 SiC+2CO↑ ( )
SiC+2CO↑ ( )
(5)SiO2+4HF===SiF4↑+2H2O ( )
A.作为玻璃的成分被消耗而使玻璃被腐蚀
B.氧化性
C.酸性氧化物的通性
D.将挥发性的酸酐从其盐中置换出来
E.未参加氧化还原反应
科目:高中化学 来源: 题型:
糕点包装中常见的脱氧剂组成为还原性铁粉、氯
化钠、炭粉 等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是
等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是
A.脱氧过程是吸热反应,可降低温度,延长糕点保质期
B.脱氧过程中铁作原电池正极,电极反应为:Fe – 3e– = Fe3+
C.脱氧过程中碳做原电池负极,电极反应为:2H2O + O2 + 4e– = 4OH–
D.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
一氧化二氯(Cl2O)是黄棕色具有强烈刺激性气味的气体。它的熔点为-116℃,沸点是3.8℃。一氧化二氯不稳定,接触一般有机物易发生爆炸;它易溶于水且易与水反应形成次氯酸溶液。制备出一氧化二氯之后,要冷却为固态才便于操作和贮存,制取少量一氧化二氯,是用干燥的氧化汞与氯气反应(同时还生成HgO·HgCl2)。制备装置如下图所示,铁架台和夹持仪器已略去。
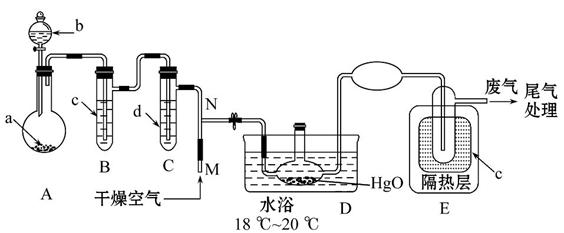
部分物质的有关资料如下:
| 化学式 | N2 | O2 | CO2 | NH3 | Cl2 |
| 熔点(℃) | -209.86 | -218.4 | -78.5 (升华) | -77.3 | -101 |
| 沸点(℃) | -195.8 | -183 | -33.35 | -34.6 |
试回答:
(1)试说明加入试剂前检验A、B、C处仪器气密性的操作方法_______ 。
(2)A中盛有的深色固体试剂a应是 ,分液漏斗中的b试剂是 。
(3)B中盛有的液体c应是 ,C中的液体d是 。
(4)D中发生反应的化学方程式是 _______。
(5)E中的保温瓶中盛有液态致冷剂c,它应是 ________(在“干冰”“冰水”
“液态空气”“液氨”“液氯”中选择一种)。在E的内管得到的Cl2O中可能含有的杂质主要是 。
(6)装置D、E间的连接方式与A、B、C间的连接方式有明显的差别,这区别是________ ,用这种不同的连接方式的主要理由是 __________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质分类的说法正确的是
A.Na2O2﹑CaO﹑K2O都是碱性氧化物 B.BaSO4﹑NaCl﹑KNO3溶液都是电解质
C.纯碱﹑烧碱﹑碱石灰都是碱 D.稀豆浆﹑果冻﹑淀粉溶液都是胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
已知三氯化铁的熔点为306℃,沸 点为315℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。某学习小组的同学对氯气与铁的反应及产物做了如下探究实验:
点为315℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。某学习小组的同学对氯气与铁的反应及产物做了如下探究实验:

(1)装置的连接顺序为 。
(2)饱和食盐水的作用是 。
(3)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:

①淡黄色溶液中加入试剂X生成淡红色溶液的离子反应方程式为_______。
②淡红色溶液中加入过量H2O2后溶液红色加深的原因是 。
(4)已知红色褪去的同时有气体生成,经检验为 O2。该小组同学对红色褪去的原因进行探究。
O2。该小组同学对红色褪去的原因进行探究。
①取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;第二份滴加试剂X,溶液出现红色;第三份滴加稀HCl和BaCl2溶液,产生白色沉淀。
②另取同浓度的 FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化。
实验①说明 ; 实验②的目的是 ;
得出结论:溶液褪色的原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
有些科学家提出硅是“21世纪的能源”,这主要是由于作为半导体材料的硅在太阳能发电过程中具有重要的作用。下列有关硅的说法中,不正确的是 ( )
A.高纯度的硅广泛用于制作计算机芯片
B.硅可由二氧化硅还原制得
C.低温时,硅与水、空气和酸不反应,但能与氢氟酸反应
D.自然界中硅的储量丰富,自然界中存在大量的单质硅
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于水玻璃的性质和用途的叙述中不正确的是( )
A .水玻璃是一种矿物胶,既不燃烧也不受腐蚀
.水玻璃是一种矿物胶,既不燃烧也不受腐蚀
B.在建筑工业上可以作黏合剂、耐酸水泥掺料
C.木材、织物浸过水玻璃后具有防腐性能且不易燃烧
D.水玻璃的化学性质稳定,在空气中不易变质
查看答案和解析>>
科目:高中化学 来源: 题型:
获取知识和信息是现代人不可缺少的能力,信息产业的飞速发展离不开材料科学的推动,信息产业的核心材料是高纯度的硅。下面是高纯度单晶硅的生产方法一:
SiO2 Si(粗硅)
Si(粗硅)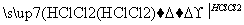 SiHCl3(沸点31.5 ℃)
SiHCl3(沸点31.5 ℃)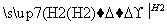 Si
Si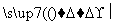 高纯硅→单晶硅
高纯硅→单晶硅
近代用得较多的另一种方法(方法二)是:用金属硅化物(Mg2Si)与盐酸作用制得硅烷(SiH4);再热分解硅烷可得高纯硅。单晶硅可用于制作大规模集成电路、整流器等,硅纯 度越高,大规模集成电路的性能越好。
度越高,大规模集成电路的性能越好。
(1)从方法一生产单晶硅的过程看,由碳还原得到的硅为何还要进一步处理?
(2)写出方法二中,生产高纯硅的两个化学方程式:
①________________________________________________________________________。
②________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com