
| A、c(CH3COO-)<c(Na+) |
| B、c(OH-)>c(H+) |
| C、c(CH3COOH)>c(CH3COO-) |
| D、c(CH3COOH)+c (CH3COO-)=0.01mol/L |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用过滤的方法除去食盐水中的泥沙 |
| B、用蒸馏的方法将自来水制成蒸馏水 |
| C、用酒精萃取碘水中的碘 |
| D、用淘洗的方法从沙里淘金 |
查看答案和解析>>
科目:高中化学 来源: 题型:
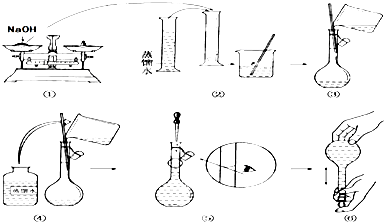
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3C00CH2CH2CH3 |
| B、CH3CH2CH2CH2 C00H |
C、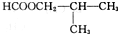 |
D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
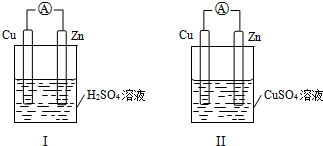
| A、装置Ⅰ,铜片上有O2逸出 |
| B、装置Ⅰ,锌片溶解,发生还原反应 |
| C、装置Ⅱ,电池反应为:Zn+Cu2+=Zn2++Cu |
| D、装置Ⅱ,外电路中,电子从铜电极流向锌电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、无色溶液中可能大量存在Al3+、NH4+、Cl-、S2- |
| B、0.1mol?L-1FeCl3溶液中大量存在Fe2+、NH4+、SCN-、SO42- |
| C、0.1mol?L-1NH4HCO3溶液中:K+、Na+、NO3-、Cl- |
| D、中性溶液中可能大量存在Fe3+、K+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
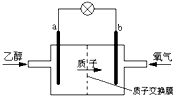 新型的乙醇电池结构如图所示,它用磺酸类质子(H+)溶剂,在200℃左右时供电,其效率比甲醇电池高出32倍,且更安全.已知电池总反应式为:C2H5OH+3O2=2CO2+3H2O.下列说法不正确的是( )
新型的乙醇电池结构如图所示,它用磺酸类质子(H+)溶剂,在200℃左右时供电,其效率比甲醇电池高出32倍,且更安全.已知电池总反应式为:C2H5OH+3O2=2CO2+3H2O.下列说法不正确的是( )| A、a极为电池的负极,该电极发生氧化反应 |
| B、电池工作时电流由b极沿导线经灯泡再到a极 |
| C、电池正极的电极反应式为:O2+2H2O+4e-=4OH- |
| D、电池工作时,1mol乙醇被氧化转移12 mol电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com