
【题目】在密闭容器里,通入x mol H2(g)和y mol I2(g),发生反应:H2(g)+I2(g)![]() 2HI(g) △H<0。达到平衡后,改变下列条件,反应速率将如何改变 (填“增大”“减小”或“不变”)?平衡将如何移动(填“向左”“向右”或“不变”)?
2HI(g) △H<0。达到平衡后,改变下列条件,反应速率将如何改变 (填“增大”“减小”或“不变”)?平衡将如何移动(填“向左”“向右”或“不变”)?
(1)升高温度,反应速率将_________,平衡将如何移动 ;
(2)加入正催化剂,反应速率将_________,平衡将如何移动 ;
(3)充入更多的H2,反应速率将_________,平衡将如何移动 ;
(4)扩大容器的体积,反应速率将_________,平衡将如何移动 ;
(5)容器体积不变,通入氖气,反应速率将___________,平衡将如何移动 ;
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示.下列分析不正确的是( ) 
A.①代表滴加H2SO4溶液的变化曲线
B.b点,溶液中大量存在的离子是Na+、OH﹣
C.c点,两溶液中含有相同量的OH﹣
D.a、d两点对应的溶液均显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】功能高分子P的合成路线如下: 
已知FnG为高分子化合物,请回答下列问题:
(1)A的分子式是C7H8 , 其结构简式是 .
(2)试剂a是 .
(3)反应③的化学方程式: .
(4)E的分子式是C6H10O2 . E中含有的官能团: .
(5)反应④的反应类型是 .
(6)反应⑤的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知乙炔(C2H2)、苯(C6H6)、乙醛(C2H4O)的混合气体中含氧元素的质量分数为8%,则混合气体中碳元素的质量分数为( )
A.84%
B.60%
C.91%
D.42%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】湿法炼锌为现代炼锌的主要方法,下列是以硫化锌精矿为原料制备单质锌的工业流程. 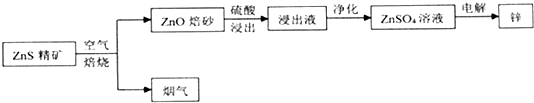
(1)烟气不能直接排放,可用于制取一种常见的强酸,该强酸为 .
(2)浸出液以硫酸锌为主,还含有Fe 3+、Fe 2+、A1 3+、Cu 2+、Cd 2+、C1一等杂质,会影响锌的电解,必须除去.净化过程如下:
①在酸性条件下,用H2O2将Fe2+氧化成Fe3+ , 离子方程式为 .
②将浸出液的pH调节为5.5左右,使Fe3+、A13+形成沉淀而除去,可选用的最佳试剂为(填字母)
A.NaOH B.NH3H2 O C.ZnOH D.H2SO4
③用Zn除去Cu2+和Cd2+
④用Ag2SO4除去Cl一 , 发生的离子方程式为, .
(3)用两支惰性电极插入500mL硫酸锌溶液中,通电电解.当电解液的pH从6.0变为3.0时(设电解时阴极没有氢气析出,且电解液在电解前后体积变化可以忽略),锌在极析出,其质量为mg.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】针对网络上流传的隔夜熟肉中因亚硝酸钠(NaNO2)含量严重超标而不能食用的说法,某兴趣小组开展如下探究活动:
活动一:查阅资料
NaNO2有毒,具有较强氧化性和较弱还原性,NaNO2溶液显碱性,国家规定肉制品中NaNO2含量不能超过30mg/kg.
(1)NaNO2溶液显碱性的原因是(用离子方程式表达)
活动二:鉴别NaNO2与食盐
(2)可用稀硫酸、淀粉和KI溶液鉴别,溶液变蓝的是(填化学式)
活动三:探究NaNO3与NaNO2的相互转化
(3)制取NaNO2与NaNO3混合溶液的装置示意图如图. 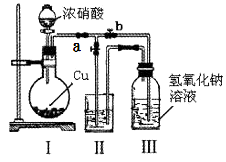
已知:2NO2+2NaOH═NaNO2+NaNO3+H2 O
①装置II中的试剂不能为水,理由是 .
②装置III中反应完全后,接下来的操作是打开活塞(选填“a”或“b”,下同),关闭活塞
(4)将NaNO2与NaNO3混合溶液露置于空气,隔夜后,测得溶液的pH减小,则溶液中NaNO2的含量(选填“增多”、“减少”、或“不变”),原因可能是(用化学方程式解释).
活动四:检测熟肉中NaNO2含量的变化
(5)分别从 1000g刚煮熟的肉和 1000g隔夜熟肉中提取NaNO2 , 配成溶液,再分别用0.00500mol/L酸性高锰酸钾溶液滴定,刚煮熟的肉消耗12.00mL,隔夜熟肉消耗16.00mL.(提示:MnO4一转化为Mn2+ , NO2一转化为NO3一)
①在该滴定实验中需要用到的实验仪器有
A.容量瓶 B.酸式滴定管 C.碱式滴定管
D.分液漏斗 E.锥形瓶 F. 烧瓶
②滴定终点的判断依据为 .
③隔夜熟肉中NaNO2的含量是mg/kg,该数据说明保存得当的隔夜熟肉(选填“能”或“不能”)食用.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,相同pH的氢氧化钠和醋酸钠溶液加水稀释,平衡时pH 随溶液体积变化的曲线如图所示,则下列叙述不正确的是( ) 
A.b、c两点溶液的导电能力不相同
B.a、b、c三点溶液中水的电离程度a>c>b
C.用相同浓度的盐酸分别与等体积的b、c处溶液反应,消耗盐酸体积Vb=Vc
D.c点溶液中C(H+)+C(CH3COOH)=C(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组同学用如图装置进行实验,一段时间后在C电极表面有铜析出,试回答下列问题.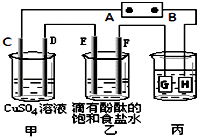
(1)B为电源的极;
(2)在电解一段时间后在甲中加入适量可以使溶液恢复到原来的浓度.
(3)在常温下,现用丙装置给铁镀铜,当丙中铁表面析出铜的3.2g时,乙中溶液的PH值为(假设溶液体积为1L);
(4)利用反应2Cu+O2+2H2SO4═2CuSO4+2H2O可制备CuSO4 , 若将该反应设计为原电池,其正极电极反应式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com