

| A.[Cu(NH3)4]SO4中所含的化学键有离子键、极性键和配位键 |
| B.[Cu(NH3)4]SO4含有NH3分子,其水溶液中也含有NH3分子 |
| C.[Cu(NH3)4]SO4的组成元素中第一电离能最大的是氧元素 |
| D.[Cu(NH3)4]SO4的外界离子的空间构型为正四面体 |
 ___________。
___________。 2NH4+ + Cu2+ + Cu + 2SO2↑ + 2H2O(2分)
2NH4+ + Cu2+ + Cu + 2SO2↑ + 2H2O(2分)
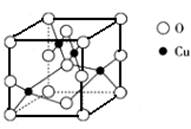
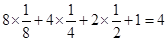 ,而铜原子为4个,即其化学式为CuO
,而铜原子为4个,即其化学式为CuO 2NH4+ + Cu2+ + Cu + 2SO2↑ + 2H2O
2NH4+ + Cu2+ + Cu + 2SO2↑ + 2H2O

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.冰溶化时,分子中H—O键发生断裂 |
| B.在晶体中只要有阳离子,一定有阴离子 |
| C.离子化合物中可能含有非极性共价键 |
| D.在SiO2晶体中,Si原子与Si—O键数目比为1:2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属键是金属阳离子和自由电子这两种带异性电荷的微粒间的强烈相互作用,所以实质与离子键类似,也是一种电性作用 |
| B.金属键可以看作是许多原子共用许多电子所形成的强烈的相互作用,所以与共价键类似,也有方向性和饱和性 |
| C.金属键是带异性电荷的金属阳离子和自由电子间的相互作用,故金属键无饱和性和方向性 |
| D.构成金属的自由电子在整个金属内部的三维空间中做自由运动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.卤化氢分子中,卤素的非金属性越强,共价键的极性越强,稳定性也越强 |
| B.以非极性键结合的分子,不一定是非极性分子 |
| C.判断A2B或AB2型分子是否是极性分子的依据是,具有极性键且分子构型不对称、键角小于180°的非直线型结构 |
| D.非极性分子中,各原子间都应以以非极性键结合 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氰分子中四原子共直线,是非极性分子 | B.氰分子中C≡N键长大于C≡C键长 |
| C.氰气分子中含有σ键和∏键 | D.氰化氢在一定条件下能与烯烃发生加成反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com