
| 0.4g |
| 40g/mol |
| 0.01mol |
| 0.400mol?L -1 |


科目:高中化学 来源: 题型:
| A、用金属钠与水或乙醇反应,比较水和乙醇分子中羟基氢(-OH)的活泼性 |
| B、用铂(Pt)电极电解Cu(NO3)2、AgNO3 混合溶液,比较铜和银的金属活泼性 |
| C、检测等物质的量浓度H3PO4和 H2SO4的酸性强弱,比较磷和硫两元素非金属性的强弱. |
| D、向无色溶液加BaCl2溶液,生成白色沉淀,再加稀硝酸,沉淀不消失,由此确定该溶液中一定含有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
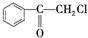 )互为同分异构体,且能发生银镜反应,分子中含有苯环、但不含-CH3的化合物有多种,它们的结构简式是
)互为同分异构体,且能发生银镜反应,分子中含有苯环、但不含-CH3的化合物有多种,它们的结构简式是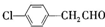 、
、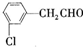 、
、 、
、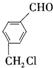 ,还有
,还有查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
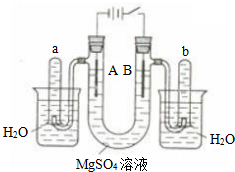 如图是一个用铂丝作电极,电解稀的MgSO4溶液的装置,电解液中加有中性红指示剂,此时溶液呈红色.(指示剂的pH变色范围:6.8~8.0,酸色-红色,碱色-黄色).
如图是一个用铂丝作电极,电解稀的MgSO4溶液的装置,电解液中加有中性红指示剂,此时溶液呈红色.(指示剂的pH变色范围:6.8~8.0,酸色-红色,碱色-黄色).查看答案和解析>>
科目:高中化学 来源: 题型:
| A、无色溶液中:K+、Na+、MnO4-、SO42- |
| B、含有大量NO3-的溶液中:NH4+、I-、SO42-、H+ |
| C、加入Al能放出H2的溶液中:Cl-、SO42-、NO3-、Mg2+ |
| D、在c(H+)=1.0×10-13mol?L-1的溶液中:Na+、SO42-、AlO-2、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、61 | B、114 |
| C、175 | D、289 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将稀氨水逐滴加入稀硫酸中,当溶液的pH=7时,c(SO42-)>c(NH4+) |
| B、两种醋酸溶液的物质的量浓度分别为c1和c2,pH的别为a和a+1,则c1=10c2 |
| C、向0.1mol?L-1的氨水中加入少量硫酸铵固体,则溶液中c(OH-)/c(NH3?H2O)增大 |
| D、pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
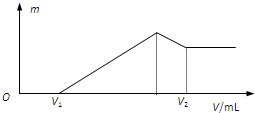 将0.1mol的镁铝混合物溶于100mL 1.5mol?L-1的H2SO4中,然后再滴加1mol?L-1的NaOH溶液.请回答:
将0.1mol的镁铝混合物溶于100mL 1.5mol?L-1的H2SO4中,然后再滴加1mol?L-1的NaOH溶液.请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com