
分析 摩尔质量以g/mol为单位,数值上等于其相对分子质量,根据n=$\frac{m}{M}$计算硫酸的物质的量,氧原子物质的量为硫酸的4倍,再根据N=nNA计算氧原子数目;根据n=$\frac{m}{M}$计算氧气的物质的量,再根据V=nVm计算氧气体积.
解答 解:硫酸的相对分子质量为98,则其摩尔质量为98g/mol,24.5g硫酸的物质的量为$\frac{24.5g}{98g/mol}$=0.25mol,则中所含的氧原子数目为0.25mol×4×6.02×1023mol-1=6.02×1023,
48g氧气物质的量为$\frac{48g}{32g/mol}$=1.5mol,标况下氧气体积为1.5mol×22.4L/mol=33.6L,
故答案为:98g/mol;6.02×1023;33.6L.
点评 本题考查物质的量有关计算、摩尔质量等,比较基础,旨在考查学生对基础知识的理解掌握.


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有②③ | B. | 只有③⑥ | C. | 除①⑤⑥ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
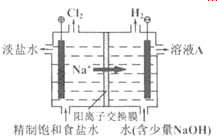 生产生活中广泛涉及氧化还原反应.
生产生活中广泛涉及氧化还原反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHSO4═Na++HSO4- | B. | NaHCO3═Na++H++CO32- | ||
| C. | KClO3═K++Cl-+3O2- | D. | Al2(SO4)3═2Al3++3SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:X2->Y->Z2+ | |
| B. | 单质的熔点:Z>W>Y | |
| C. | 能破坏水的电离平衡的离子为:Y-,Z2+,W- | |
| D. | 离子化合物ZX的熔点高,ZX可作为耐火材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com