
| A、加酚酞显无色的溶液 |
| B、含有H+的溶液 |
| C、pH<7的溶液 |
| D、CH3COOH和NH3?H2O混合液,当c(CH3COO-)>c(NH4+)时 |


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案科目:高中化学 来源: 题型:
| A、2.65 g |
| B、2.96 g |
| C、6.56g |
| D、5.3g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| X |
| Cl2 |
| O2 |
| O2 |
| H2O |
| A、当X是强碱时,A、B、C、D、E、F均含同一种元素 |
| B、当X是强酸时,A、B、C、D、E、F均含同一种元素 |
| C、B和Cl2的反应是氧化还原反应 |
| D、当X是强酸时,C在常温下是气态单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、S(g)+O2═SO2(1);|△H|>297.3kJ/mol |
| B、S(g)+O2═SO2(1);|△H|<297.3kJ/mol |
| C、1molSO2的键能总和小于1molS和1molO2键能之和 |
| D、1molSO2的键能总和等于1molS和1molO2键能之和 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2SO4滴入NaAlO2溶液中 |
| B、Ba(OH)2溶液滴入Al2(SO4)3溶液中 |
| C、NaOH溶液滴入Al2(SO4)3溶液中 |
| D、氨水滴入Al2(SO4)3溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平均相对分子质量减小 |
| B、N2O4的转化率提高 |
| C、压强为原来的2倍 |
| D、颜色变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、NH4Br的电子式: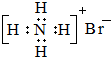 | ||
B、S原子的结构示意图: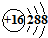 | ||
| C、乙醇的结构简式:C2H6O | ||
D、原子核内有18个中子的氯原子:
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同压强、同温度的O2和O3 |
| B、同温度、同体积的NH3和N2 |
| C、同体积、同密度的C2H4和C3H6 |
| D、同压强、同体积的N2O和CO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com