
| A. | 该溶液中,Na+、Fe3+、NO3-、Cl-可能大量共存 | |
| B. | 和溴水反应的离子方程式:Br2+SO32-+H2O=2H++2Br-+SO42- | |
| C. | 和Ba(OH)2溶液加热反应的离子方程式:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | 1L0.1mol•L-1该溶液和足量的硝酸充分反应,生成2.24L(标准状况)SO2气体 |
分析 A.(NH4)2SO3溶液中存在亚硫酸根离子,铁离子能够氧化亚硫酸根离子;
B.溴单质能够将亚硫酸根离子氧化硫酸根离子;
C.漏掉了生成亚硫酸钡的反应;
D.二者反应生成硫酸铵,不会生成二氧化硫气体.
解答 解:(NH4)2SO3在溶液中电离出铵根离子和亚硫酸根离子,
A.Fe3+具有氧化性,能够氧化亚硫酸根离子,在溶液中不能大量共存,故A错误;
B.亚硫酸铵和溴水反应生成硫酸铵和溴化氢,反应的离子方程式为:Br2+SO32-+H2O=2H++2Br-+SO42-,故B正确;
C.(NH4)2SO3和Ba(OH)2溶液加热反应生成氨气、亚硫酸钡和水,正确的离子方程式为:Ba2++SO32-+2NH4++2OH-$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+BaSO3↓,故C错误;
D.稀硝酸具有强氧化性,将亚硫酸根离子氧化成硫酸根离子,不会生成二氧化硫气体,故D错误;
故选B.
点评 本题考查了离子共存的判断、离子方程式和化学方程式书写,题目难度中等,注意掌握离子反应发生条件、离子方程式和化学方程式的书写原则,明确离子共存的判断方法,D为易错点,注意反应生成硫酸铵,不会生成二氧化硫.


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:多选题
| A. | E(3s)>E(3p)>E(3d) | B. | E(3s)>E(2s)>E(1s) | C. | E(4f)>E(3d)>E(4s) | D. | E(5s)>E(4s)>E(4f) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
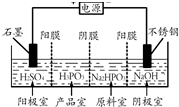 亚磷酸(H3PO3)可用作检测汞、金、银、铅、碘酸等的分析试剂.
亚磷酸(H3PO3)可用作检测汞、金、银、铅、碘酸等的分析试剂.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述元素中,Y的原子半径最大 | |
| B. | 上述元素中,W的气态氢化物最稳定 | |
| C. | 元素W和X可形成含有极性键的极性分子WX3 | |
| D. | 工业上可用电解熔融的Y、Z的化合物的方法冶炼Y、Z的单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
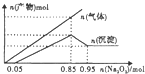
| A. | 混合溶液中m(Al3+)为5.4g | B. | 混合溶液中c(Mg2+)为0.5mol/L | ||
| C. | 混合溶液的pH=2 | D. | 混合溶液中c(Cl-)为1.7mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
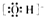
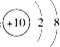

| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正丁烷和异丁烷互为同分异构体 | |
| B. | 乙醇和乙酸都能与氢氧化钠溶液反应 | |
| C. | 淀粉和蛋白质的水解产物都是氨基酸 | |
| D. | 葡萄糖和蔗糖都能发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素Z可与元素X形成共价化合物XZ2 | |
| B. | 元素X与氢形成的原子比为1:1的化合物有很多种 | |
| C. | 元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成 | |
| D. | 元素W、X的氯化物中,各原子均满足8电子的稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作和现象 | 结论 |
| A | CH4和Cl2混合于试管中光照,颜色逐渐褪去 | 二者发生了化合反应 |
| B | 微热滴有2滴酚酞的饱和NaHCO3溶液,溶液颜色加深 | NaHCO3受热分解生成了Na2CO3 |
| C | 向淀粉溶液中加入20%的硫酸,加热几分钟,冷却后再加入银氨溶液,水浴,没有银镜生成 | 淀粉没发生水解 |
| D | 向装有Fe(NO3)2溶液的试管中加入稀硫酸,观察到试管口有红棕色气体产生 | 酸性环境下,NO3-被Fe2+还原为NO,NO遇氧气生成NO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com