
分析 蓄电池在充电和放电时发生的反应是:NiO2+Fe+2H2O$?_{充电}^{放电}$Fe(OH)2+Ni(OH)2,放电时原电池反应负极反应为:Fe-2e-+2OH-=Fe(OH)2,原电池的正极为:NiO2+2e-+2H2O=Ni(OH)2+2OH-,充电池,电极反应为原电池的逆反应,以此解答该题.
解答 解:(1)该电池放电时,原电池的正极为:NiO2+2e-+2H2O=Ni(OH)2+2OH-,溶液中氢氧根离子难度增大,所以正极附近溶液的pH增大;
故答案为:增大;
(2)充电时,阳极发生氧化反应,Ni(OH)2被氧化生成NiO2,电极方程式为Ni(OH)2-2e-+2OH-=NiO2+2H2O,故答案为:Ni(OH)2-2e-+2OH-=NiO2+2H2O.
点评 本题考查了原电池、电解池原理的分析判断和应用,为高频考点,注意根据电池总反应中元素的化合价的变化判断,注意电极方程式的书写方法,题目难度中等,侧重于学生的分析能力的考查.


科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1NaAlO2溶液:H+、Na+、Cl-、SO42- | |
| B. | pH=11的溶液中:CO32-、Na+、AlO2-、NO3-、S2-、SO32- | |
| C. | 水电离的H+浓度为10-12mol•L-1的溶液中:Cl-、CO32-、NO3-、SO32- | |
| D. | 使甲基橙变黄的溶液中:Fe2+、MnO4-、NO3-、Na+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 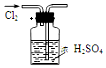 干燥Cl2 | B. |  吸收HCl | ||
| C. |  用自来水制蒸馏水 | D. |  吸收NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它们的分子数目之比为1:1 | B. | 它们所含氧原子数目之比为2:3 | ||
| C. | 它们所含原子数目之比为3:4 | D. | 它们的质量之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非金属氧化物一定是酸性氧化物 | |
| B. | 能与酸反应生成盐和水的氧化物一定是碱性氧化物 | |
| C. | 分子中含有几个氢原子就是几元酸 | |
| D. | 酸性氧化物不一定是非金属氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 粗铜电解精炼时,电解质溶液的组成和浓度均保持不变 | |
| B. | 铁制品上镀一定厚度的锌层,选用锌作阳极,镀件作阴极,含锌离子的溶液作电解液 | |
| C. | 电解氯化钠溶液可以制备金属钠 | |
| D. | 氯碱工业中,电解饱和食盐水时,阳极上产生Cl2和NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用pH试纸能测得氯水的pH=4 | |
| B. | 胶体区别于其他分散系的本质特征是分散质的微粒直径在1-100nm之间 | |
| C. | 所有的金属都是固态的 | |
| D. | 用平行光线照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可使用溴水鉴别植物油和汽油 | |
| B. | 利用二氧化碳制造全降解塑料,可以消除温室效应 | |
| C. | “玉兔号”月球车上的太阳能电池的材料是硅 | |
| D. | 实验室金属钠失火时,可使用泡沫灭火器灭火 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com