
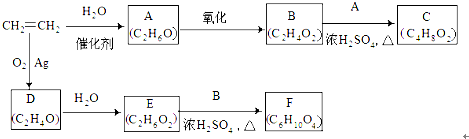
 E
E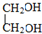 F
F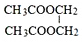 写出C酸性条件下水解的方程式CH3COOCH2CH3+H2O$?_{△}^{稀H_{2}SO_{4}}$CH3COOH+CH3CH2OH
写出C酸性条件下水解的方程式CH3COOCH2CH3+H2O$?_{△}^{稀H_{2}SO_{4}}$CH3COOH+CH3CH2OH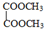 .
. 分析 根据各物质的转化关系 及有关物质的分子式可知,乙烯与水加成生成A,A为乙醇,乙醇催化氧化生成B,B为CH3COOH,乙酸与乙醇反应生成C,C为乙酸乙酯,乙烯与氧气反应生成D(C2H4O),D为环状化合物,所以D为环氧乙烷 ,根据E和F的分子式及B的结构可知,E与乙酸发生酯化反应按1:2反应,D→E是开环加成反应,故E为
,根据E和F的分子式及B的结构可知,E与乙酸发生酯化反应按1:2反应,D→E是开环加成反应,故E为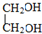 ,乙二醇与乙酸反应生成F(C6H10O4),F为二乙酸乙二酯
,乙二醇与乙酸反应生成F(C6H10O4),F为二乙酸乙二酯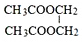 ,据此解答.
,据此解答.
解答 解:根据各物质的转化关系 及有关物质的分子式可知,乙烯与水加成生成A,A为乙醇,乙醇催化氧化生成B,B为CH3COOH,乙酸与乙醇反应生成C,C为乙酸乙酯,乙烯与氧气反应生成D(C2H4O),D为环状化合物,所以D为环氧乙烷 ,根据E和F的分子式及B的结构可知,E与乙酸发生酯化反应按1:2反应,D→E是开环加成反应,故E为
,根据E和F的分子式及B的结构可知,E与乙酸发生酯化反应按1:2反应,D→E是开环加成反应,故E为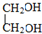 ,乙二醇与乙酸反应生成F(C6H10O4),F为二乙酸乙二酯
,乙二醇与乙酸反应生成F(C6H10O4),F为二乙酸乙二酯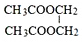 ,
,
(1)根据上面的分析可知,A的名称为乙醇,其中的 官能团为-OH,
故答案为:乙醇;-OH;
(2)A+B→C的反应为乙酸与乙醇反应生成乙酸乙酯,化学方程式为CH3COOH+CH3CH2OH $?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O,
故答案为:CH3COOH+CH3CH2OH $?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O;
(3)A为乙醇,A被Cu催化氧化的方程式为 2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O;
(4)A为乙醇,A在一定条件下可生成CH2=CH2,反应方程式为CH3CH2OH $→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2+H2O,
故答案为:CH3CH2OH $→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2+H2O;
(5)根据上面的分析可知,D为环氧乙烷 ,E为
,E为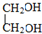 ,F为
,F为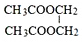 ,C酸性条件下水解的方程式为CH3COOCH2CH3+H2O$?_{△}^{稀H_{2}SO_{4}}$ CH3COOH+CH3CH2OH,
,C酸性条件下水解的方程式为CH3COOCH2CH3+H2O$?_{△}^{稀H_{2}SO_{4}}$ CH3COOH+CH3CH2OH,
故答案为: ;
;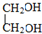 ;
;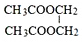 ;CH3COOCH2CH3+H2O$?_{△}^{稀H_{2}SO_{4}}$ CH3COOH+CH3CH2OH;
;CH3COOCH2CH3+H2O$?_{△}^{稀H_{2}SO_{4}}$ CH3COOH+CH3CH2OH;
(6)F为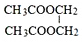 ,F的同系物M,其分子式为C4H6O4,且核磁共振氢谱只有一个峰,则M的结构简式为
,F的同系物M,其分子式为C4H6O4,且核磁共振氢谱只有一个峰,则M的结构简式为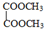 ,
,
故答案为: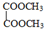 .
.
点评 本题考查有机推断,涉及烯烃、醇、醛、羧酸等性质以及学生推理能力等,是对有机化合物知识的综合考查,能较好的考查考生的思维能力,根据乙烯与D的分子式,判断D的结构是解题的关键,难度中等,是高考热点题型.


 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:解答题
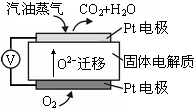 淮南是我国重要的煤炭生产基地,通过煤的气化和液化,能使煤炭得以更广泛的应用.
淮南是我国重要的煤炭生产基地,通过煤的气化和液化,能使煤炭得以更广泛的应用.| t/min | 0 | 1 | 2 | 3 | 4 |
| n(H2O)/mol | 1.20 | 1.04 | 0.90 | 0.70 | 0.70 |
| n(CO)/mol | 0.80 | 0.64 | 0.50 | 0.30 | 0.30 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 浓度/mol•L-1 时间/min | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| l0 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.017 | 0.034 |
| 50 | 0.032 | 0.017 | 0.034 |
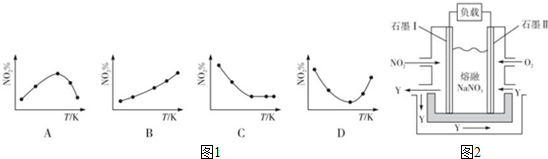
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无机物的种类比有机物多 | |
| B. | 互为同系物的有机物有可能同时互为同分异构体 | |
| C. | 丁烷有两种同分异构体 | |
| D. | 醇和醚均互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯中的甲苯:加溴水分液 | |
| B. | 乙醇中的水:加新制CaO蒸馏 | |
| C. | 甲烷中的乙烯:用溴的四氯化碳溶液洗气 | |
| D. | 乙酸乙酯中的乙酸:加饱和Na2CO3溶液分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用量筒量取浓盐酸配制0.01mol/L稀盐酸时,量筒用蒸馏水洗净后未经干燥直接量取浓盐酸 | |
| B. | 配制稀盐酸定容时,俯视容量瓶刻度线 | |
| C. | 滴定前尖嘴处无气泡,滴定终点时有气泡 | |
| D. | 滴定过程中用少量蒸馏水将锥形瓶内避粘附的盐酸冲下 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
| CH3COOH | 1.8×10-5 | HCN | 5×10-10 |
| H2CO3 | Ka1=4.2×10-7 | HClO | 3×10-8 |
| Ka2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸和浓盐酸长期暴露在空气中浓度都会降低,但原理不相同 | |
| B. | 常温下,浓硫酸可以用铁制容器储存,说明铁与冷的浓硫酸不反应 | |
| C. | 向某溶液中加入盐酸酸化的氯化钡溶液,生成白色沉淀,说明原溶液中一定含有SO42- | |
| D. | 向某溶液中滴加氯水后,再加入KSCN溶液,溶液呈红色,说明原溶液中一定含有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铜与稀硫酸反应:O2-+2H+═H2O | |
| B. | Na投入水中:Na+H2O═Na++OH-+H2↑ | |
| C. | 铜与浓硝酸的反应:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| D. | 氢氧化钡与稀硫酸的反应:H++2SO42-+2Ba2++OH-═2BaSO4↓+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com