
����Ŀ���ҹ�������Ա��Zn�ͼ⾧ʯ������ﮣ�ZnMn2O4��Ϊ�缫���ϣ����Ƴ�һ��ˮϵп���ӵ�ء��õ�ص��ܷ�Ӧ����ʽ��xZn +Zn1-xMn2O4![]() ZnMn2O4(0<x<1��������˵����ȷ����
ZnMn2O4(0<x<1��������˵����ȷ����
A. ZnMn2O4�Ǹ�������
B. ���ʱ��Zn2+��ZnMn2O4�缫Ǩ��
C. ���ʱ��������Ӧ��ZnMn2O4-xZn2+-2xe-=Zn1-x Mn2O4
D. ��ŵ�����У�ֻ��ZnԪ�صĻ��ϼ۷����仯
���𰸡�C
��������A. ԭ���ӷŵ���Znʧ���ӷ���������Ӧ��Ϊ�������ϣ���A����B. ���ʱ��ԭ��Ϊ���ԭ�������ʱԭ���ĸ������ӵ�Դ�ĸ�����ΪZn����Zn2+��������Zn�缫Ǩ�ƣ���B����C. ���ʱ������ZnMn2O4������������Zn1-x Mn2O4����缫��ӦΪZnMn2O4-xZn2+-2xe-=Zn1-x Mn2O4����C��ȷ��D. ��ŵ�����У�ֻ��ZnԪ�صĻ��ϼ۽��ͣ�MnԪ�صĻ��ϼ����ߣ���D����ΪC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1���������ı仯�ͷ�Ӧ�Ŀ����ȽǶ��о���Ӧ��2H2 + O2 = 2H2O�� ��֪�÷�ӦΪ���ȷ�Ӧ����ͼ����ȷ��ʾ�÷�Ӧ�������仯����________�����A����B����
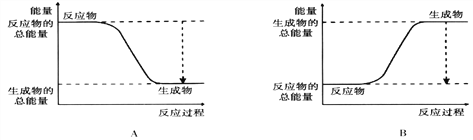
�Ӷϼ��ͳɼ��ĽǶȷ���������Ӧ�������ı仯����ѧ���ļ������±���
��ѧ�� | H��H | O��O | H��O |
����kJ/mol | 436 | 496 | 463 |
������1molˮ���Էų����� _____kJ
��2�����·�Ӧ����ľ̿��ˮ�Ʊ�ˮú�� ������طֽ� ��ըҩ��ը ���������кͷ�Ӧ ����ʯ����ˮ��������ʯ�� �� Ba(OH)2��8H2O��NH4Cl ����̬ˮҺ�������ڷ��ȷ�Ӧ���У�
_________________������ţ���д����Ӧ�Ļ�ѧ����ʽ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������ܱ������У��������»�ѧ��Ӧ��
CO2(g) +H2(g)![]() CO (g) +H2O (g)
CO (g) +H2O (g)
�仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
t�� | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�ش��������⣺
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK�� ��
��2���÷�ӦΪ________��Ӧ(����ȡ������ȡ�)��
��3����˵���÷�Ӧ�ﵽ��ѧƽ��״̬����________��
A��������ѹǿ���� B�����������c(CO)����
C��v��(H2)��v��(H2O) D��c(CO2)��c(CO)
��4��ij�¶��£�ƽ��Ũ�ȷ�����ʽ�� 3c(CO2)��c(H2)��5c(CO)��c(H2O)�����жϴ�ʱ���¶�Ϊ ����
��5�� 830��ʱ����1L�ܱ������зֱ�Ͷ��lmolH2��lmolCO2��Ӧ�ﵽ��ѧƽ��ʱ��CO2��ת����Ϊ �������¶Ȳ��䣬��ƽ����ϵ���ٳ���1molH2��lmolCO2���´ﵽ��ѧƽ��ʱ��CO2��ƽ��ת���� (���������С�����䡱)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ClO2��Ϊһ�ֹ����͵�����������������ȡ��Cl2��Ϊ����ˮ������������֪ClO2��һ��������ˮ���������л��ܼ������壬ʵ�����Ʊ�ClO2��ԭ�������������ƹ�����������Ӧ ��2NaClO2 + Cl2 ===2ClO2 + 2NaCl��
��ͼ��ʵ���������Ʊ����ռ�һ�����ϴ�����ClO2��װ�ã�ijЩ�г�װ�ú͵����Ʒʡ�ԣ�������E��ʢ��CCl4Һ�壨���ڳ�ȥClO2�е�δ��Ӧ��Cl2����
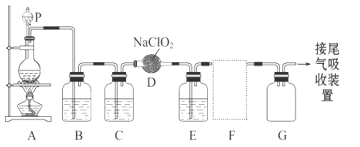
��1������P��������______________________��
��2��д��װ��A����ƿ�ڷ�����Ӧ�����ӷ���ʽ��_____________________��
��3��Bװ������ʢ�Լ���____________________��
��4��FΪClO2�ռ�װ�ã�Ӧѡ�õ�װ����______________������ţ���������Eװ�õ��������ĵ��ܿ���__________����ӿ���ĸ����
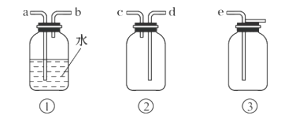
��5������100 mL 2 mol��L-1��Ũ������������MnO2�Ʊ�Cl2����������HCl�����ʵ�����________������ţ���
A.��0.1 mol B.0.1 mol C.��0.1 mol D.���ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ������ ��
A. ���³�ѹ����8gO2����16NA������
B. 1 molL-1MgCl2��Һ�к��������Ӹ���Ϊ2NA
C. ʢ��SO2���ܱ������к���NA����ԭ�ӣ���SO2�����ʵ���Ϊ0.5mol
D. ���³�ѹ�£�22.4L��NO2��CO2������庬��2NA��Oԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶�ʱ����2 L���ܱ������У�X��Y��Z�������ʵ�����ʱ��ı仯��������ͼ��ʾ��

(1)��ͼ���������ݽ��з������÷�Ӧ�Ļ�ѧ����ʽΪ_______________��
(2)��Ӧ�ӿ�ʼ��2minĩ����Z(Ϊ��̬)��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ_______ mol/(L��min)��
(3)����Ӧ���е���_____minʱ���÷�Ӧ�ﵽƽ�⡣��Ӧ�ﵽƽ������д�ʩһ���ܼӿ컯ѧ��Ӧ���ʵ���____
A������Z���� B�������¶�
C��ʹ�������� D������X��Y����
(4)�ֱ���X��Y�ķ�Ӧ��������ʾ�Ѵﵽ��ѧƽ��״̬�ı���ʽΪ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NaHSO3��Һ�ڲ�ͬ�¶��¾��ɱ�����KIO3��������NaHSO3��ȫ���ļ���I2����������I2��������ʱ��������NaHSO3�ķ�Ӧ���ʡ���Ũ�Ⱦ�Ϊ0.020 mol��L-1NaHSO3(����������)10.0 mL��KIO3(����)������Һ40.0 mL��ϣ���¼10~55������Һ����ʱ�䣬55��ʱδ�۲쵽��Һ������ʵ��������ͼ����ͼ�����������ж�����ȷ����
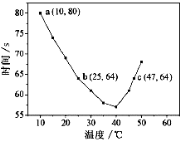
A��40��֮ǰ��40��֮����Һ������ʱ�����¶ȵı仯�����෴
B��ͼ��b��c�����Ӧ��NaHSO3��Ӧ���ʲ���
C��ͼ��a���Ӧ��NaHSO3��Ӧ����Ϊ5.0 ��10-5mol��L-1��s-1
D���¶ȸ���40��ʱ���������������������ָʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ijѧ��Ϊ��̽��п�����ᷴӦ�����е����ʱ仯������100mLϡ�����м���������п�ۣ�����ˮ�������ռ���Ӧ�ų���������ʵ���¼���£��ۼ�ֵ����
ʱ�䣨min�� | 1 | 2 | 3 | 4 | 5 |
���������mL/SPT�� | 50 | 120 | 232 | 290 | 310 |
(1)����ʱ����У���0��1��1��2��2��3��3��4��4��5 min����Ӧ����������
_____________min������Ҫԭ����_____________��
(2)��2��3����ʱ����������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ����__________________ ��
(3)�����Ӧ̫���ң�Ϊ�˼�����Ӧ���ʶ��ֲ����ٲ����������������������зֱ����������������Һ������Ϊ���е��ǣ����ţ� __________ ��
A������ˮ B��NaCl��Һ C��Na2CO3��Һ D��CuSO4��Һ
����ijͬѧ��ͬ����Ԫ�����ʵݱ����ʵ��ʱ���Լ�����ˡ���ʵ�鷽��������¼���й�ʵ���������±�(���еġ�ʵ�鷽�����롰ʵ������ǰ�����Ƕ�Ӧ��ϵ)
ʵ�鷽�� | ʵ������ |
����ɰֽ�����þ�����ˮ��Ӧ������ӦҺ�еμӷ�̪ | A������ˮ�棬�۳�С����ˮ���������ƶ�����֮��ʧ����Һ��ɺ�ɫ�� |
��������з�̪��Һ����ˮ��Ӧ | B�������������������������ڿ�����ȼ�գ���Һ���dz��ɫ�� |
��þ����2mol/L���ᷴӦ | C����Ӧ��ʮ�־��ң���������������ڿ�����ȼ�ա� |
��������2mol/L���ᷴӦ | D�����ɰ�ɫ��״�������̶�������ʧ�� |
�����Ȼ�����Һ�еμ�����������Һ������ | E�����ҷ�Ӧ����������������ڿ�����ȼ�ա� |
���������ͬѧ���������ʵ�鱨��
(1)ʵ��Ŀ�ģ�_________________��
(2)ʵ����Ʒ����������ɰֽ�����Թܣ��۽�ͷ�ιܣ��ܾƾ��ƣ����ԹܼС��Թܼܣ�����ֽ�������ӣ���С�����Უ��Ƭ������ƿ(100mL)�ȣ�
ҩƷ���ơ�þ����������2mol/L�������ᡢAlCl3��Һ������������Һ�ȡ�
(3)��д��ʵ�鷽�����Ӧ��ʵ������(���ϱ���ʵ��������ѡ��)��������й����ӷ���ʽ
ʵ�鷽�� | ʵ������(��д��ĸ����) | �й����ӷ���ʽ |
�� | _________ | Mg+2H2O(��ˮ)==Mg(OH)2+H2�� |
�� | _________ | _____________________ |
�� | _________ | Mg+2H+==Mg2++H2�� |
�� | _________ | ___________________ |
�� | _________ | Al3+ + 3OH- = Al(OH)3�� |
___________________ |
(4)ʵ����ۣ�_____________________
(5)��ͬѧ�ڱ�ʵ�������ȥm�˴����壬��Ӧ��Ϻ�����ʣ�࣬���ռ���VL����(SPT)�£���ͬѧ����˹����ԭ�����ı���ʽΪ________���ú�m��V��ʽ�ӱ�ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ijԪ�صĻ��ϼ��ɻ���̬��Ϊ����̬�������� ��
A.�п��ܱ�������Ҳ�п��ܱ���ԭ
B.������
C.�ɸ۱�Ϊ���
D.����ԭ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com