
下列说法正确的是:①Cl-的结构示意图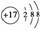 ②羟基的电子式:·
②羟基的电子式:·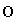 H; ③HClO的结构式:H—Cl—O;④NaHCO3在水中的电离方程式:NaHCO3===Na++H++CO; ⑤Na2O的水溶液能导电,这不能说明Na2O是电解质; ⑥SiO2既能与氢氟酸反应又能与NaOH溶液反应,故SiO2是两性氧化物;⑦分馏、干馏、裂化都是化学变化( )
H; ③HClO的结构式:H—Cl—O;④NaHCO3在水中的电离方程式:NaHCO3===Na++H++CO; ⑤Na2O的水溶液能导电,这不能说明Na2O是电解质; ⑥SiO2既能与氢氟酸反应又能与NaOH溶液反应,故SiO2是两性氧化物;⑦分馏、干馏、裂化都是化学变化( )
A.①②⑤ B.①④⑥⑦ C.②③④⑥ D.②③⑤⑥⑦
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
无色有刺激性气味的SO2气体与含1.5 mol Cl的一种含氧酸(该酸的某盐常用于实验室制取氧气)的溶液在一定条件下反应,可生成一种强酸和一种氧化物,若有1.5NA个电子转移时,该反应的化学方程式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA代表阿伏加德罗常数的数值,下列说法正确的是( )
A.12.5mL 16mol·L-1浓硫酸与足量锌反应,转移电子数为0.2NA
B.0.1 mol24Mg18O晶体中所含中子总数为2.0 NA
C.1L 1 mol·L-1的醋酸溶液中离子总数为2NA
D.4.5 g SiO2晶体中含有的硅氧键数目为0.3 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中含有HCO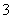 、SO
、SO 、CO
、CO 、CH3COO-4种阴离子.若向其中加入足量的Na2O2后,溶液中离子浓度基本保持不变的是 ( )
、CH3COO-4种阴离子.若向其中加入足量的Na2O2后,溶液中离子浓度基本保持不变的是 ( )
A.CH3COO- B.SO
 C.CO
C.CO D.HCO
D.HCO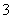
查看答案和解析>>
科目:高中化学 来源: 题型:
常见的 五种盐A、B、C、D、E,它们
五种盐A、B、C、D、E,它们 的阳离子可能是Na+、NH
的阳离子可能是Na+、NH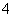 、Cu2+、Ba2+、Al3+、Ag+、Fe
、Cu2+、Ba2+、Al3+、Ag+、Fe 3+,阴离子可能是Cl-、NO
3+,阴离子可能是Cl-、NO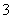 、SO
、SO 、CO
、CO ,已知:
,已知:
①五种盐均溶于水,水溶液均为无色。
②D的焰色反应呈黄色。
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈 碱性。
碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失。
⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀。
请回答下列问题:
(1)五种盐中,一定没有的阳离子是____________;所含阴离子相同的两种盐的化学式是 。
(2)D的化学式为_________,D溶液显碱性的原因是(用离子方程式表示):
。
(3)E和氨水反应的离子方程式是___________________________________ _____。
(4)设计实验检验B中所含的阳离子:
。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室里常用干燥剂有:①浓硫酸(98%);②无水氯化钙;③变色硅胶[硅胶的主要成分是二氧化硅,在其中掺入少量的无水氯化钴(CoCl2)做指示剂,无水氯化钴呈蓝色,吸水后变为CoCl2·6H2O,呈粉红色];④五氧化二磷;⑤碱石灰(主要成分是氢氧化钠、氧化钙,制法是:把生石灰加到浓的烧碱溶液中,再加强热蒸干)等。
(1)写出制取干燥剂碱石灰过 程中有关反应的化学方程式。
程中有关反应的化学方程式。
________________________________________________________________________。
(2)上述物质中,属于纯净物的是( )
A.①②④ B.②④
B.②④
C.①②④⑤ D.全部
(3)上述干燥剂 中,不宜用于干燥氯化氢气体的是________。
中,不宜用于干燥氯化氢气体的是________。
(4)上述干燥剂①~④,其主要化学成分依次属于______________(填各物质所属的类别)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于溶液和胶体的叙述,正确的是( )
A.溶液是电中性的,胶体是带电的
B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
C.溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动
D.一束光线分别通过溶液和胶体时,后者会出现 明显的光带,前者则没有
明显的光带,前者则没有
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质在指定条件下电离方程式正确的是 ( )
A.Na2CO3溶于水 Na2CO3===Na+CO
B.Al(OH)3酸式电离 Al(OH)3===H++AlO+H2O
C.NaHS溶于水HS-的电离 HS-+H2O H2S+OH-
H2S+OH-
D.NaHCO3加热熔化 NaHCO3===Na++HCO
查看答案和解析>>
科目:高中化学 来源: 题型:
某物质M具有热导率高、高温下电绝缘性好、高温下材料强度大、无毒等优异性能.经检测,M中只含有两种短周期元素.现取82gM溶于适量的NaOH溶液中恰好反应,得到无色溶液A和44.8L气体B(气体体积为标准状况下),该气体能使红色石蕊试纸变蓝.往反应后的溶液中逐滴加入盐酸,可观察到溶液先变浑浊后变澄清.
物质B有如下转化关系:BCD EE是一种强酸.将c和D的混合物溶解在接近零度的水中,即可得到一种弱酸F的水溶液.请回答下列问题:
EE是一种强酸.将c和D的混合物溶解在接近零度的水中,即可得到一种弱酸F的水溶液.请回答下列问题:
(1)物质M的化学式为 ,属于 晶体(填“分子”、“离子”、“原子”等).
(2)无色溶液A呈碱性,其原因是 (用离子方程式表示).
(3)弱酸F是一种比醋酸酸性稍强的弱酸,很不稳定,通常在室温下易分解.要制得F溶液,可以往冷冻的其钠盐浓溶液中加入或通入某种物质,下列物质不适合使用的是 (填序号).
a.盐酸 b.二氧化碳 c.稀硫酸 d.二氧化硫
(4)工业碱性废水中若含有NO﹣2,可用铝粉除去.已知此反应体系中检测到B气体.写出上述反应的离子方程式 .若改用电解法将废水中NO﹣2转换为N2除去,N2将在 (填“阴极”或“阳极”)生成,电极反应为 .
(5)现发现一种活性很强的化合物G,其组成为NH5,G遇水能产生两种气体,其中一种气体为B,则物质G的电子式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com