
【题目】已知 2NO(g)+O2(g)2NO2(g) H<0,若该反应在绝热、恒容的密闭体系中进行,则下列示意图能说明在t1时刻达到平衡状态的是 ( )
a. 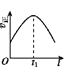 b.
b.  c.
c. 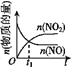 d.
d. 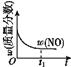
A.abB.bcC.bdD.cd
科目:高中化学 来源: 题型:
【题目】如图把气体缓慢通过盛有足量试剂的试剂瓶M,在试管N中可以观察到明显现象的是
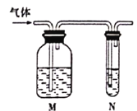
选项 | 气体 | M中试剂 | N中试剂 |
A | SO2、CO2 | 酸性KMnO4溶液 | 品红溶液 |
B | Cl2、HCl | 浓硫酸 | 淀粉-KI溶液 |
C | NH3、CO2 | 浓硫酸 | 酚酞试液 |
D | C2H4、CH4 | 酸性KMnO4溶液 | 溴的CCl4溶液 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】G是一种治疗急慢性呼吸道感染的特效药中间体,其制备路线如图:

(1)化合物C中的含氧官能团是_____。
(2)A→B的反应类型是______。
(3)化合物F的分子式为C14H21NO3,写出F的结构简式______。
(4)从整个制备路线可知,反应B→C的目的是______。
(5)同时满足下列条件的B的同分异构体共有_______种。
①分子中含有苯环,能与NaHCO3溶液反应;
②能使FeCl3溶液显紫色
(6)根据已有知识并结合相关信息,完成以![]() 、CH3NO2为原料制备
、CH3NO2为原料制备 的合成路线图____(无机试剂任用,合成路线流程图示例见本题题干)。
的合成路线图____(无机试剂任用,合成路线流程图示例见本题题干)。
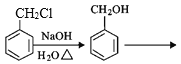
 ,其中第二步反应的方程式为_____。
,其中第二步反应的方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 均为原子序数小于18的常见元素,且原子序数依次增大。已知
均为原子序数小于18的常见元素,且原子序数依次增大。已知![]() 原子最外层电子数与核外电子总数之比为
原子最外层电子数与核外电子总数之比为![]() ,
,![]() 原子的最外层电子数与次外层电子数之比为
原子的最外层电子数与次外层电子数之比为![]() ;
;![]() 比
比![]() 的原子序数小1;
的原子序数小1;![]() 与
与![]() 的电子层结构相同;化合物
的电子层结构相同;化合物![]() 在常温下为气体。请回答下列问题:
在常温下为气体。请回答下列问题:
(1)写出![]() 的简单离子的结构示意图:______。
的简单离子的结构示意图:______。
(2)由![]() 、
、![]() 、
、![]() 三种元素形成的盐的化学式为____________。
三种元素形成的盐的化学式为____________。
(3)![]() 与
与![]() 可形成2种分子,分别为10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式:____________。
可形成2种分子,分别为10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式:____________。
(4)写出![]() 的单质的一种工业用途:____________。
的单质的一种工业用途:____________。
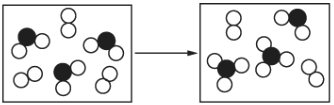
(5)如图表示由上述元素中的某两种元素组成的气体分子在密闭容器中,一定条件下充分反应前后的转化关系,该转化过程的化学方程式为____________。
(6)![]() 是由
是由![]() 、
、![]() 、
、![]() 、
、![]() 四种元素组成的一种化合物,已知
四种元素组成的一种化合物,已知![]() 既能与盐酸反应,又能与
既能与盐酸反应,又能与![]() 溶液反应,还能和氯水反应,写出
溶液反应,还能和氯水反应,写出![]() 与氯水反应的离子方程式:__________________。
与氯水反应的离子方程式:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)分别写出由氧在一定条件下生成下列物质的化学方程式(必须注明反应条件)。
①Na2O2_______________。
②Na2O__________________。
(2)KO2能吸收CO2生成K2CO3和O2,故可用作特殊情况下的氧气源,试写出该反应的化学方程式:_____________________。
(3)活泼金属复杂的氧化物(如过氧化物、超氧化物等)在一定条件下都可以生成氧气,从而用作特殊情况下的氧气源。现有下列四种物质,你认为在运输鱼苗的时候用(________)作为氧气源更合适?理由是:_________ 。
A.Na2O2 B.K2O2 C.KO2 D.CaO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知短周期主族元素X、Y、Z、W的原子序数依次增大,X元素原子的最外层电子数是内层电子数的3倍,Y与X能形成两种化合物,Z所在的周期序数与族序数相同。下列说法正确的是( )
A.Y的单质能从Z的盐溶液中置换出Z
B.简单氢化物的热稳定性:![]()
C.Z与X两元素不能形成阴离子
D.简单离子的半径大小:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为四种常见元素,其中X、Y、Z为短周期元素。有关信息如表所示.
原子或分子相关信息 | 单质或化合物相关信息 | |
X |
| X的最高价氧化物对应的水化物为无机酸中的最强酸 |
Y | Y原子的最外层电子数等于电子层数 | Y的氧化物是典型的两性氧化物,可用于制造一种极有前途的高温材料 |
Z | Z原子的最外层电子数是次外层电子数的 | Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料 |
W | W原子的最外层电子数小于4 | W的常见化合价有 |
(1)W在周期表中的位置为______,![]() 在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为______
在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为______
(2)X的简单阴离子的结构示意图为______,X的最高价氧化物对应水化物的水溶液与Y的氧化物反应的离子方程式为________
(3)Z的氧化物在通讯领域用来作______,工业上制备Z的单质的化学反应方程式为______。锗与Z是同一主族元素,它可用来制造半导体品体管.研究表明:有机锗具有明显的抗肿瘤活性,锗不与![]() 溶液反应但在有
溶液反应但在有![]() 存在时可与
存在时可与![]() 溶液反应生成锗酸盐,反应的化学方程式为_______
溶液反应生成锗酸盐,反应的化学方程式为_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是应用广泛的金属,以铝土矿(主要成分为A12O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如图:

已知:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为__。
(2)“滤渣Ⅰ”的成分有___。
(3)向“过滤Ⅰ”所得滤液中通入足量的CO2,反应的离子方程式为___。
(4)“滤液Ⅱ”中加入足量的CaO,生成的__(填化学式)可循环利用。
(5)“灼烧”的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析核电荷数为1 ~ 18的元素原子的核外电子层数和最外层电子数,回答下列问题:
(1)核电荷数为6和14的元素原子,它们的____________相同,____________不相同;核电荷数为15和16的元素原子,它们的____________相同,____________不相同;核电荷数为10和18的元素原子,它们的最外层电子数均为____________,它们的元素符号分别是____________、____________。
(2)某元素的原子核外有三个电子层,最外层电子数是核外电子总数的![]() ,该元素的元素符号是____________,原子结构示意图是____________。
,该元素的元素符号是____________,原子结构示意图是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com