
| A. | 室温下,CH3COONa和CaCl2混合溶液:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) | |
| B. | 相同温度下,0.6 mol•L-1氨水和0.3 mol•L-1氨水中c(OH-)之比是2:1 | |
| C. | 向0.1 mol•L-1NaNO3溶液中滴加盐酸使溶液的pH=5,此时混合液中的c(Na+)=c(NO3-) | |
| D. | 室温下,0.1 mol•L-1NH4Cl溶液与0.1 mol•L-1氨水等体积混合(pH>7):则c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-) |
分析 A.根据混合液中的物料守恒c(Na+)=c(CH3COO-)+c(CH3COOH)、2c(Ca2+)=c(Cl-)判断;
B.氨水浓度越大,一水合氨的电离程度越小;
C.钠离子和硝酸根离子不发生反应,根据物料守恒可得:c(Na+)=c(NO3-);
D.混合液呈碱性,说明一水合氨的电离程度大于铵根离子的水解程度,则c(NH4+)>c(NH3•H2O).
解答 解:A.由物料守恒可知:c(Na+)=c(CH3COO-)+c(CH3COOH),2c(Ca2+)=c(Cl-),则c(Na+)+2c(Ca2+)=c(CH3COO-)+c(CH3COOH)+c(Cl-),故A错误;
B.相同温度下,由于0.6 mol•L-1氨水的电离程度比0.3 mol•L-1氨水的电离程度小,则两溶液中c(OH-)之比小于2:1,故B错误;
C.向0.1 mol•L-1NaNO3溶液中滴加盐酸使溶液的pH=5,由于钠离子和硝酸根离子不水解,根据物料守恒可知:c(Na+)=c(NO3-),故C正确;
D.室温下,0.1 mol•L-1NH4Cl溶液与0.1 mol•L-1氨水等体积混合(pH>7),混合液呈碱性,则一水合氨的电离程度大于铵根离子的水解程度,故c(NH4+)>c(NH3•H2O),结合物料守恒可知:c(NH4+)>c(Cl-)>c(NH3•H2O),溶液中正确的粒子浓度大小为:c(NH4+)>c(Cl-)>c(NH3•H2O)>c(OH-),故D错误;
故选C.
点评 本题考查了离子浓度大小比较,题目难度中等,明确反应后溶质组成为解答关键,注意掌握电荷守恒、物料守恒、盐的水解原理等知识在判断离子浓度大小中的应用方法.


 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案科目:高中化学 来源: 题型:解答题
 .
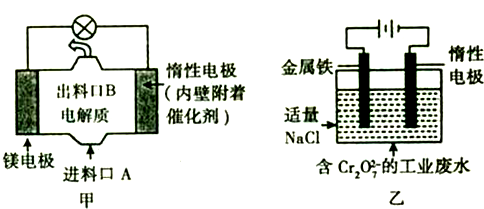
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠、钾着火时用水灭火 | |
| B. | 点燃氢气前要验纯,点燃甲烷前不必验纯 | |
| C. | 浓NaOH溶液溅到皮肤上,立即用水冲洗,然后涂上浓硫酸 | |
| D. | 稀释浓硫酸时,为防止液体飞溅,将浓硫酸沿烧杯壁缓缓加入水中,并不断搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | CO | H2 | |||
| I | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
| II | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
| III | 900 | 2 | 1 | a | b | t |
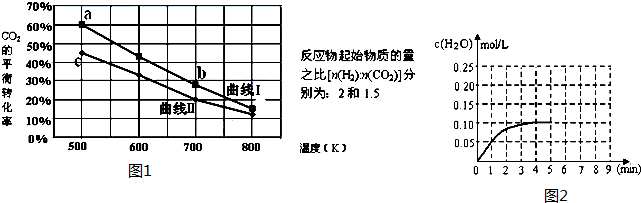
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
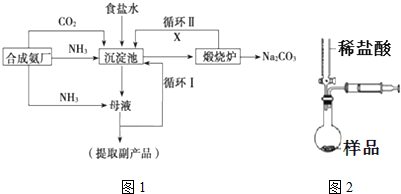
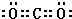 ,沉淀池中发生的化学反应方程式为:CO2+NH3+NaCl+H2O═NaHCO3↓+NH4Cl.
,沉淀池中发生的化学反应方程式为:CO2+NH3+NaCl+H2O═NaHCO3↓+NH4Cl.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
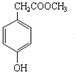 的分子式是C9H10O3,1mol化合物I完全燃烧,消耗10mol氧气.
的分子式是C9H10O3,1mol化合物I完全燃烧,消耗10mol氧气.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 7.8gNa2O2和 Na2S混合物中所含阴离子的数目为0.1NA | |
| B. | 0.1mol丙烷中含有的共价键数目为0.8NA | |
| C. | 标准状况下,11.2LSO2中含有分子的数目为0.5NA | |
| D. | t℃,MgCO3的Kap=4×14-4,则饱和饱和溶液中含Mg2+数目为2×10-3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5:3 | B. | 5:4 | C. | 1:1 | D. | 3:5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com