
| A. | P4和NO2都是共价化合物 | B. | CCl4和NH3分子中都含有极性键 | ||
| C. | CaO和SiO2都是离子化合物 | D. | Na2O2是离子化合物,只含有离子键 |
分析 A.P4是单质;
B.两种不同非金属原子之间形成极性键;
C.以离子键结合形成的化合物属于离子化合物;
D.过氧化钠中O与O之间形成共价键.
解答 解:A.P4是单质,不是化合物,NO2中只含有共价键是共价化合物,故A错误;
B.两种不同非金属原子之间形成极性键,CCl4中含有C-H极性键,NH3分子中含有N-H极性键,故B正确;
C.以离子键结合形成的化合物属于离子化合物,CaO属于离子化合物,SiO2属于共价化合物,故C错误;
D.Na2O2中含有离子键属于离子化合物,过氧化钠中O与O之间形成共价键,故D错误.
故选B.
点评 本题考查化学键,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注重基础知识的考查,题目难度不大.


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:解答题
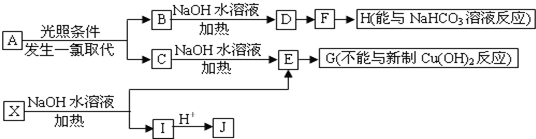
 、
、 、
、 .(不包括A,写结构简式)
.(不包括A,写结构简式) ;反应类型是酯化反应.
;反应类型是酯化反应. +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$ +
+ +H2O
+H2O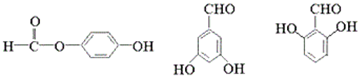 任意一种.
任意一种.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ;
;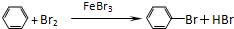 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由非电解质溶于水得到的溶液 | |
| B. | 将pH=9的烧碱溶液稀释100倍所得到的溶液 | |
| C. | 等物质的量的强酸与强碱反应得到的溶液 | |
| D. | c(H+)、c(OH-)均为5.0×10-7mol•L-1的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl MgCl2 NH4Cl | B. | H2O Na2O ? CO2 | ||
| C. | NH3 H2O CO2 | D. | CaCl2 ? NaOH H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9 | B. | 8 | C. | 17 | D. | 25 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
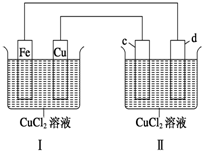
| A. | Ⅰ和Ⅱ无外加电源,都是原电池 | |
| B. | 铁为负极,d为阴极,两个电极上都发生还原反应 | |
| C. | Ⅰ中铜电极Ⅱ中c电极上有铜析出 | |
| D. | Ⅰ是原电池,Ⅱ是电解池 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯、苯、乙醇均能使酸性高锰酸钾溶液褪色 | |
| B. | 乙烯和聚丙烯都能与氢气在一定条件下发生加成反应 | |
| C. | 煤制煤气是化学变化,是高效、清洁地利用煤的重要途径 | |
| D. | 乙酸乙酯、油脂、葡萄糖、蛋白质都可以发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
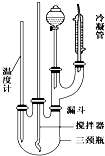 硝基苯是一种重要的化工原料,其制备原理是:
硝基苯是一种重要的化工原料,其制备原理是: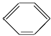 +HO-NO2$→_{50~60℃}^{H_{2}SO_{4}}$
+HO-NO2$→_{50~60℃}^{H_{2}SO_{4}}$ 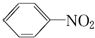 +H2O△H<0
+H2O△H<0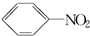 +HO-NO2$→_{△}^{H_{2}SO_{4}}$
+HO-NO2$→_{△}^{H_{2}SO_{4}}$ 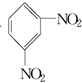 +H2O
+H2O查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com