
| A. | 氯化钡有两性 | |
| B. | 两支试管的白色沉淀均为亚硫酸钡 | |
| C. | SO2既有还原性,又是酸性氧化物 | |
| D. | 溶液的碱性增强,增大SO2在水溶液中的溶解度,使SO32-浓度增大 |
分析 二氧化硫为酸性氧化物,具有还原性,二氧化硫与氢氧化钠反应生成亚硫酸钠,亚硫酸钠能够与氯化钡反应生成亚硫酸被沉淀,二氧化硫能够与氯水反应生成硫酸,硫酸与氯化钡反应生成硫酸钡沉淀,据此解答.
解答 解:在氯化钡溶液中通入SO2,溶液澄清,若将氯化钡溶液分盛两支试管中,一支加入氯水,二氧化硫能够与氯水反应生成硫酸,硫酸与氯化钡反应生成硫酸钡沉淀,体现二氧化硫的还原性,
另一支加烧碱溶液,然后再通入SO2,二氧化硫与氢氧化钠反应生成亚硫酸钠,亚硫酸钠能够与氯化钡反应生成亚硫酸被沉淀,体现二氧化硫的酸性氧化物的性质,
所以通过实验体现SO2有还原性,是酸性氧化物.
故选:C.
点评 本题考查了物质的性质,熟悉二氧化硫的还原性与酸性氧化物的性质是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
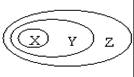 表中所示物质或概念间的从属关系符合右图的是( )
表中所示物质或概念间的从属关系符合右图的是( )| X | Y | Z | |
| A | 钠元素 | 主族元素 | 短周期元素 |
| B | 非电解质 | 化合物 | 纯净物 |
| C | 氯化铁 | 胶体 | 分散系 |
| D | 置换反应 | 氧化还原反应 | 放热反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
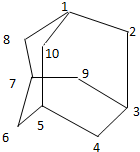 石油中溶有一种碳氢化合物-金刚烷.金刚烷 是一种环状烃,它的结构高度对称.下图表示金刚烷,图中数字是碳原子编号.碳原子用小黑点表示,氢原子均省略,一条短线表示共用一对电子.
石油中溶有一种碳氢化合物-金刚烷.金刚烷 是一种环状烃,它的结构高度对称.下图表示金刚烷,图中数字是碳原子编号.碳原子用小黑点表示,氢原子均省略,一条短线表示共用一对电子.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、Na+、SON32-、I- | B. | Mg2+、Na+、CO32-、Br- | ||
| C. | Al3+、Mg2+、I-、SO32- | D. | Al3+、CO32-、Br-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌粒与稀硫酸的反应 | |
| B. | 灼热的木炭与CO2反应 | |
| C. | 甲烷在氧气中的燃烧反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com