
【题目】甲、乙两烧杯中各盛有200mL3mol·L-1的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后,测得生成的气体体积比为V(甲)∶V(乙)=1∶2,则加入铝粉质量为( )
A.10.8gB.7.2gC.5.4gD.3.6g
【答案】A
【解析】
铝与盐酸反应的化学方程式是2Al+6HCl═2AlCl3+3H2↑,铝与氢氧化钠反应的化学方程式是2Al+2NaOH+2H2O═2NaAlO2+3H2↑;根据题意,盐酸、氢氧化钠物质的量相等,若盐酸、氢氧化钠都完全反应,则生成气体体积比为V(甲)∶V(乙)=1∶3,若两份铝都完全反应,则生成氢气体积相等,实际生成氢气体积比V(甲)∶V(乙)=1∶2,说明乙中氢氧化钠有剩余、甲中铝有剩余。
盐酸和氢氧化钠溶液中溶质的物质的量均为0.2L×3mol/L=0.6mol,根据以上分析,甲中铝有剩余,盐酸完全反应,设铝与酸反应时生成的氢气的物质的量为xmol,
则 2Al+6HCl═2AlCl3+3H2↑
6 3
0.6mol x
![]() ,X=0.3mol,测得生成的气体体积比为V(甲)∶V(乙)=1∶2,则乙生成氢气的物质的量是0.6mol,设乙中参加反应的铝为ymol,
,X=0.3mol,测得生成的气体体积比为V(甲)∶V(乙)=1∶2,则乙生成氢气的物质的量是0.6mol,设乙中参加反应的铝为ymol,
则2Al+2NaOH+2H2O═2NaAlO2+3H2↑
2 3
y 0.6mol
![]() ,解得y=0.4mol,则铝的质量为0.4mol×27g/mol=10.8g;
,解得y=0.4mol,则铝的质量为0.4mol×27g/mol=10.8g;
故选A。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ.在锌与某浓度的盐酸反应的实验中,实验员得到下面的结果:
锌的质量(g) | 锌的形状 | 温度(℃) | 溶解于酸花的时间(s) | |
A | 2 | 薄片 | 5 | 400 |
B | 2 | 薄片 | 15 | 200 |
C | 2 | 薄片 | 25 | 100 |
D | 2 | 薄片 | 35 | 50 |
E | 2 | 薄片 | 45 | 25 |
F | 2 | 粉末 | 15 | 5 |
(1)写出实验中发生反应的离子方程式:___________,该反应是_____反应(填“放热”或“吸热”);
(2)仔细观察A~F的实验数据对比,你可以得到关于温度影响反应速率结论,用此结论,计算:55℃时,2g锌薄片溶解于酸中需花____ s。
(3)对比结果B与F,解释结果F那么快的原因:________
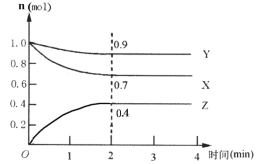
Ⅱ.某可逆反应在某体积为5L的密闭容器中进行,在从0~4分钟各物质的量的变化情况如图所示(X、Y、Z均为气体)。
(1)该反应的的化学方程式为_______;
(2)反应开始至2分钟时,X的平均反应速率为______;
(3)能说明该反应已达到平衡状态的是______;
a.每消耗3molX,同时消耗1molY
b.容器内压强保持不变
c.Z的浓度不再变化
d.容器内混合气体的密度保持不变
(4)由下图求得平衡时Y的转化率为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家哈迈德·泽维尔研究运用激光技术观察化学反应时分子中原子的运动,在研究中证实光可诱发如图所示的变化。下列叙述不正确的是

A.两物质的分子式相同
B.两物质均可发生加成反应
C.两物质分子中所有原子不可能处于同一平面上
D.两物质都不能生成高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)我国化工专家侯德榜的“侯氏制碱法” 又叫“联合制碱法”以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱Na2CO3,有关反应的化学方程式:
(1)____;
(2)____。
(II).取一定量的酸性KMnO4溶液依次进行下列实验,有关现象记录如下:①滴加适量H2O2,紫红色褪去,并有气泡产生;②再加入适量的PbO2固体,固体溶解,溶液又变为紫红色; ③最后通入足量的SO2气体。请回答下列问题:
(1)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为__;
(2)实验③中的现象为__;
(3)实验①、②中反应的离子方程式分别是__、___。
(III)铝与NaOH溶液反应同温同压下,在体积和浓度均为100mL2mol·L1的盐酸和NaOH溶液中各加入等质量的Al,产生气体的体积之比为5∶6,则所加Al的质量为__g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:
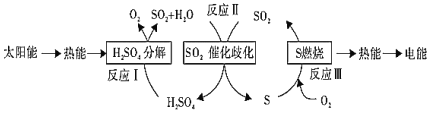
(1)反应Ⅰ:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ·mol-1
反应Ⅲ:S(s)+O2(g)![]() SO2(g) ΔH3=-297 kJ·mol-1
SO2(g) ΔH3=-297 kJ·mol-1
写出反应Ⅱ的热化学方程式:_____________________。
(2)歧化反应可简单理解为化学反应中同一反应物中某元素化合价同时出现升降。已知I-离子可以作为水溶液中SO2歧化反应的催化剂。有关离子方程式如下(未配平):
a.SO2+I-+H+→S↓+I2+H2O
b.I2+H2O+SO2→SO42-+H++I-
i.依据图示及以上离子方程式a、b,写出SO2歧化反应方程式:______________。
ii.探究a、b反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
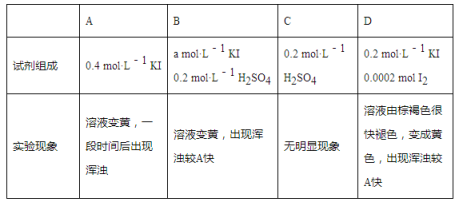
①B是A的对比实验,则a=__________。
②比较A、B、C,可得出的结论是______________________。
③实验表明,SO2的歧化反应速率D>A,结合①、②反应速率解释原因:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲用NaOH固体配制1.0mol·L-1的NaOH溶液240mL:
(1)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却
其正确的操作顺序为___。必须用到的玻璃仪器有烧杯、玻璃棒、___。
(2)某同学欲称量NaOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的态如图所示。烧杯的实际质量为___g,要完成本实验该同学应称出___gNaOH。
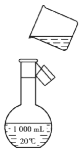
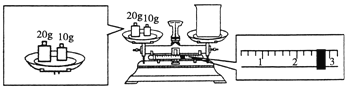
(3)使用容量瓶前必须进行的一步操作是___。
(4)如图是该同学转移溶液的示意图,图中有两处错误,请写出:
①____;
②____;
(5)在配制过程中,下列操作会引起误差偏高的是___(填字母)。
A.所用NaOH已经潮解
B.向容量瓶加水定容时眼睛俯视液面
C.转移时没有洗涤玻璃棒和烧杯
D.溶解后溶液没有冷却至室温就转移
E.容量瓶没有干燥处理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中书写正确的是( )
A.用小苏打治疗胃酸过多:![]()
B.氢氧化钡溶液与稀硫酸反应:![]()
C.碳酸氢钙溶液和氢氧化钠溶液混合:![]()
D.铜片插入硝酸银溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲酸(HCOOH)是还原性酸,又称作蚁酸,常用于橡胶、医药、染料、皮革等工业生产。某化学兴趣小组在分析甲酸的组成和结构后,对甲酸的某些性质进行了探究。请回答下列问题。
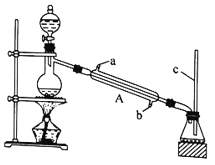
I.甲酸能与醇发生酯化反应
该兴趣小组用如上图所示装置进行甲酸(HCOOH)与甲醇(CH3OH)的酯化反应实验:
有关物质的性质如下:
沸点/℃ | 密度(g·cm-3) | 水中溶解性 | |
甲醇 | 64.5 | 0.79 | 易溶 |
甲酸 | 100.7 | 1.22 | 易溶 |
甲酸甲酯 | 31.5 | 0.98 | 易溶 |
(1)装置中,仪器A的名称是_________________,长玻璃管c的作用是__________________________。
(2)甲酸和甲醇进行酯化反应的化学方程式为____________________________________________。
(3)要从锥形瓶内所得的混合物中提取甲酸甲酯,可采用的方法为__________________________________。
II.甲酸能脱水制取一氧化碳

(1)利用上图装置制备并收集CO气体,其正确的连接顺序为a→__________(按气流方向从左到右,用小写字母表示)。
(2)装置B的作用是__________________________________。
(3)一定条件下,CO能与NaOH固体发生反应:CO+NaOH ![]() HCOONa。
HCOONa。
①为了证明“CO与NaOH固体发生了反应”,设计下列定性实验方案:取固体产物,配成溶液,___________。
②测定产物中甲酸钠(HCOONa)的纯度:准确称取固体产物8,0g配制成100mL溶液,量取20.00mL该溶液于锥形瓶中,再加入___________作指示剂,用1.5mol/L的盐酸标准溶液滴定剩余的NaOH,平行滴定三次,平均消耗盐酸的体积为5.05mL,则产物中甲酸钠的质量分数为_______(计算结果精确到0.1%)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究几种气态氧化物的性质,某同学设计了以下实验:用三只集气瓶收集二氧化硫、二氧化氮气体,倒置在水槽中。然后,分别缓慢通入适量氧气或氯气,如图所示。一段时间后,A、B装置中集气瓶充满溶液,C装置中集气瓶里还有气体。

(1)如果装置A中通入的氧气恰好使液体充满集气瓶,假设瓶内液体不扩散。
①写出A中总反应的化学方程式:________;该实验对工业上生产硝酸的启示是________。
②假设该实验条件下,气体摩尔体积为aL·mol-1,集气瓶中溶液的物质的量浓度为________。
(2)实验前在C水槽里滴加几滴紫色石蕊试液,通入氧气前后,实验现象变化可能为___________;写出化学方程式:________,溶液充满集气瓶后,在B水槽里滴加硝酸钡溶液,可能观察到的现象为___________;写出所有反应的离子方程式:_________;证明B水槽反应后溶液里有氯离子的操作方法是______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com